Metoject®, Auto-injecteur, solution injectable en stylo pré-rempli
Information destinée aux patients en Suisse
Qu’est-ce que METOJECT AUTO-INJECTEUR et quand doit-il être utilisé ?
Le principe actif de Metoject est le méthotrexate.
1 ml de solution injectable contient 50 mg de méthotrexate (sous la forme de méthotrexate disodique)
Le méthotrexate est un analogue de l’acide folique avec les propriétés suivantes:
– en tant qu’anti-métabolite il bloque la division des cellules qui se divisent rapidement,
– en tant qu’immunosuppresseur il inhibe, respectivement affaiblit, les réactions de défense indésirables de l’organisme,
– en tant qu’antiphlogistique il possède des propriétés anti-inflammatoires.
Metoject Auto-injecteur est utilisé sur prescription médicale lors de:
– polyarthrite active chronique (arthrite rhumatoïde) chez l’adulte,
– formes poly-arthritiques de l’arthrite juvénile active sévère, en l’absence de réponse aux anti-inflammatoires non stéroïdiens (AINS),
– psoriasis vulgaire sévère, tenace et invalidant, en cas de réponse insuffisante à d’autres formes thérapeutiques telles que photothérapie, PUVA et rétinoïdes, ainsi qu’arthrite psoriasique sévère chez l’adulte,
– formes légères à modérées de la maladie de Crohn chez les patients adultes lorsqu’un traitement adéquat par d’autres médicaments n’est pas possible.
L’arthrite rhumatoïde est une maladie inflammatoire chronique du tissu conjonctif, caractérisée par une inflammation du tissu synovial (revêtement interne des articulations). Ce tissu sécrète un liquide qui sert de lubrifiant à de nombreuses articulations. L’inflammation du tissu synovial est responsable d’un épaississement de ce tissu et de la tuméfaction consécutive des articulations concernées.
L’arthrite juvénile touche les enfants et les adolescents en dessous de 16 ans. On parle de polyarthrite lorsque cinq articulations ou plus sont touchées au cours des six premiers mois de la maladie.
Le psoriasis vulgaire est une maladie chronique de la peau, qui se caractérise par l’apparition de placards squameux rougeâtres et blanchâtres.
Le psoriasis arthropathique se manifeste dans le cadre d’un psoriasis. Il se manifeste par des lésions psoriasiformes de la peau et des ongles. Ce sont essentiellement les articulations des doigts et des orteils qui sont concernées.
Metoject Auto-injecteur interfère avec le processus évolutif de la maladie et ralentit ce dernier.
La maladie de Crohn est un type de maladie inflammatoire des intestins qui peut affecter n’importe quelle région du tractus gastro-intestinal et provoquer des symptômes tels que des douleurs abdominales, de la diarrhée, des vomissements ou une perte de poids.
Pour le traitement de la polyarthrite rhumatoïde, du psoriasis et de la maladie de Crohn, il faut absolument veiller à utiliser la dose recommandée 1x par semaine; si la dose recommandée est prise une fois par jour par inadvertance, cela peut entraîner des intoxications sévères dont l’évolution est parfois fatale.
Quand METOJECT AUTO-INJECTEUR ne doit-il pas être utilisé ?
– lorsque vous êtes hypersensible (allergique) au méthotrexate ou à l’un des composants de Metoject Auto-injecteur,
– lorsque vous souffrez d’affections hépatiques ou rénales (voir également le paragraphe «Comment utiliser Metoject Auto-injecteur?»),
– lorsque vous souffrez de maladies du système hématopoïétique (formation du sang),
– lorsque vous consommez beaucoup d’alcool,
– lorsque vous souffrez d’infections graves, telles que notamment la tuberculose, le VIH ou autres syndromes de l’immunodéficience,
– lorsque vous avez des ulcères dans la région de la bouche, de l’estomac ou de l’intestin,
– lorsque vous êtes enceinte ou désirez l’être,
– lorsque vous allaitez,
– lorsque vous devez être vacciné simultanément avec des vaccins vivants (p. ex. rougeole, oreillons, rubéole, poliomyélite ou varicelle),
– après un certain type d’anesthésie (anesthésie au gaz hilarant).
Quelles sont les précautions à observer lors de l’utilisation de METOJECT AUTO-INJECTEUR ?
Ce médicament peut affecter les réactions, l’aptitude à la conduite et l’aptitude à utiliser des outils ou des machines!
Il faut être prudent lors de l’utilisation de Metoject Auto-injecteur si vous devez subir une intervention chirurgicale sous anesthésie (anesthésie au gaz hilarant).
Certains types d’anesthésiants ont une influence sur l’effet du méthotrexate et peuvent entraîner des effets secondaires graves d’issue fatale. Informez votre médecin si vous deviez avoir besoin d’une opération sous anesthésie (anesthésie au gaz hilarant).
Mesures de précaution spéciales pour le traitement par Metoject Auto-injecteur
Le méthotrexate affecte temporairement la production du sperme et des ovules, ces effets étant réversibles dans la plupart des cas. Le méthotrexate peut provoquer des fausses couches et de graves malformations congénitales. Si vous êtes une femme, vous devez éviter de tomber enceinte pendant le traitement par le méthotrexate et pendant au moins six mois après l’arrêt du traitement. Si vous êtes un homme, vous devez éviter de concevoir un enfant au moment du traitement et pendant au moins trois mois après l’arrêt du traitement par le méthotrexate (voir aussi la rubrique «Metoject peut-il être utilisé pendant la grossesse ou l’allaitement?»).
Même lorsque Metoject Auto-injecteur est utilisé à de faibles doses, des effets indésirables graves peuvent survenir. Afin de reconnaître ces effets à temps, des mesures de précaution doivent être prises et des contrôles réguliers doivent être effectués par le médecin après le début du traitement.
Contrôles de suivi et précautions recommandés:
Avant le début du traitement:
Des examens sanguins doivent être effectués afin de contrôler si vous avez suffisamment de globules sanguins, de procéder à des tests en vue de contrôler les enzymes du foie, la bilirubine (produit de la dégradation de l’hémoglobine), la sérumalbumine (une protéine du sang) et la fonction rénale.
Le médecin décidera éventuellement si d’autres examens du foie sont nécessaires. Il peut s’agir d’une imagerie de votre foie ou du prélèvement d’un petit échantillon de tissu du foie pour un examen plus approfondi.
Votre médecin contrôlera également si vous souffrez de tuberculose ou d’hépatite et procédera à une radiographie du thorax.
Pendant le traitement:
Des contrôles sont effectués (au moins chaque mois pendant les six premiers mois et au moins trimestriellement par la suite):
– Recherche de modifications des muqueuses dans la cavité buccale et le pharynx.
– Examen sanguin.
– Contrôle de la fonction hépatique (foie) et des enzymes hépatiques dans le sérum.
En cas d’une augmentation persistante des enzymes hépatiques, une réduction du dosage, voire l’interruption du traitement devront être envisagés. Pendant le traitement par méthotrexate, aucun autre médicament pouvant altérer les fonctions du foie ou le système hématopoïétique (formation du sang) ne doit être utilisé. Si un tel traitement s’avérait néanmoins nécessaire, des contrôles rapprochés devront être effectués.
Vous ne devez pas consommer d’alcool pendant le traitement.
– Éventuellement, réalisation d’examens d’imagerie pour surveiller l’état du foie.
– Éventuellement, prélèvement d’un petit échantillon de tissu du foie pour un examen plus approfondi.
– Contrôle de la fonction rénale: Le méthotrexate étant éliminé par les reins, des effets graves au niveau rénal peuvent survenir si la fonction rénale est altérée (en particulier chez les patients âgés). Dans de tels cas, une surveillance médicale particulièrement vigilante est indiquée.
– Contrôle de la fonction respiratoire et le cas échéant test fonctionnel pulmonaire : En fonction du résultat de ce test, le traitement par méthotrexate devra éventuellement être suspendu.
Il est très important que vous vous rendiez à ces examens planifiés. Si les résultats de l’un de ces examens sont anormaux, votre médecin adaptera votre traitement en conséquence.
– Le méthotrexate peut avoir une influence sur votre système immunitaire ainsi que sur les résultats de vos vaccinations et tests immunologiques. Des infections chroniques inactives (notamment zona, tuberculose, hépatite B ou C) pourront notamment être réactivées. Vous ne devez pas être vacciné par des vaccins vivants pendant le traitement par Metoject Auto-injecteur.
Des réactions inflammatoires de la peau (dermatite) ou un coup de soleil, provoqués par une irradiation, peuvent réapparaître au cours du traitement par le méthotrexate (réaction de réactivation). Des modifications de la peau causées par un psoriasis (lésions psoriasiques) peuvent s’aggraver lors d’une exposition aux rayons UV et de l’administration simultanée de méthotrexate.
Metoject Auto-injecteur peut avoir comme effet secondaire une diarrhée. Dans ce cas, le traitement doit être interrompu. Veuillez contacter votre médecin si vous souffrez d’une diarrhée.
La tuméfaction des ganglions lymphatiques (lymphomes) peut rendre nécessaire l’arrêt du traitement. Si les lymphomes ne régressent pas spontanément, un traitement approprié devra être instauré.
Une encéphalopathie (modifications pathologiques du cerveau) / leucoencéphalopathie (modification pathologique de la substance blanche du cerveau) a été observée chez des patients cancéreux traités par le méthotrexate et ne peut pas être exclue lors d’un traitement par le méthotrexate pour d’autres maladies.
Chez les personnes âgées, la fonction rénale et/ou hépatique peut être diminuée et les réserves d’acide folique peuvent être réduites (voir paragraphe «Comment utiliser Metoject Auto-injecteur?»)
Si vous consommez régulièrement et concomitamment de l’alcool, ou si vous avez recours à d’autres médicaments pouvant altérer la fonction hépatique ou la formule sanguine (notamment le léflunomide), le risque de toxicité hépatique sera accru sous méthotrexate. Dans de tels cas, vous devez être soumis à des contrôles médicaux vigilants. Ceci est également à prendre en considération si vous utilisez en même temps à des médicaments hématotoxiques (qui altèrent la formation du sang) (p. ex. le léflunomide). Lorsque le léflunomide et le méthotrexate sont associés, le risque d’apparition d’une pancytopénie (réduction du nombre de cellules sanguines et des plaquettes) et d’une hépatotoxicité (altération du foie) est accru.
Les antibiotiques tels que la pénicilline, les glycopeptides, les sulfonamides, la ciprofloxacine et la céfalotine, peuvent dans des cas isolés réduire l’excrétion rénale du méthotrexate. Ceci a pour conséquence une augmentation des concentrations sanguines du méthotrexate et peut conduire à une toxicité hématologique (concernant la formation du sang) et gastro-intestinale (concentrant l’estomac et l’intestin).
Le probénécide et les acides organiques faibles tels que les diurétiques de l’anse et les pyrazolés (phénylbutazone) peuvent augmenter les concentrations sanguines du méthotrexate. Les anti-inflammatoires non stéroïdiens (AINS) et l’acide salicylique peuvent augmenter le risque d’une insuffisance rénale.
Si vous prenez des médicaments qui réduisent l’excrétion du méthotrexate, qui sont responsables d’une insuffisance rénale, ou qui réduisent potentiellement la formation du sang, vous serez soumis à des contrôles médicaux plus stricts.
Si vous prenez en même temps des médicaments ayant des effets secondaires possibles sur la moelle épinière (p. ex. sulfonamides, triméthoprime-sulfaméthoxazole, chloramphénicol, pyriméthamine), on peut observer une perturbation accrue de la formation sanguine.
Si vous prenez des médicaments responsables d’une carence en folate (p. ex sulfonamides, triméthoprime-sulfaméthoxazole), la toxicité du méthotrexate pourra être augmentée. Il faut donc être particulièrement vigilant s’il existe chez vous une carence connue en acide folique. Votre médecin décidera alors de la nécessité d’une administration supplémentaire d’acide folique.
Une toxicité accrue du méthotrexate n’est pas attendue lors de l’administration de Metoject Auto-injecteur avec d’autres traitements de fond antirhumatismaux (p. ex. sels d’or, pénicillamine, hydroxychloroquine, sulfasalazine, azathioprine, cyclosporine).
L’association du méthotrexate et de la sulfasalazine peut conduire au renforcement de l’action du méthotrexate. Dès lors que le méthotrexate et la sulfasalazine sont des inhibiteurs de la synthèse de l’acide folique des effets secondaires peuvent survenir. Ceci n’a toutefois été décrit que rarement jusqu’ici.
Si des inhibiteurs de la pompe à protons sont administrés concomitamment, on peut observer des interactions médicamenteuses. Lorsque l’inhibiteur de la pompe à protons oméprazole est administré, l’élimination rénale du méthotrexate peut être retardée. En association avec le pantoprazole, c’est l’élimination du métabolite 7-hydroxyméthotrexate qui est retardée, ce qui a conduit dans un cas à des myalgies (douleurs musculaires et malaise) et à des frissons.
Des saignements aigus des poumons chez des patients atteints d’une maladie rhumatismale sous-jacente ont été rapportés avec le méthotrexate. Contactez immédiatement votre médecin si vous observez des symptômes tels que des expectorations sanguinolentes ou une toux avec expectorations de sang.
Interactions avec d’autres médicaments et avec l’alcool
Pendant votre traitement par Metoject Auto-injecteur, il faut dans la mesure du possible ne pas boire d’alcool. Evitez la consommation excessive de boissons riches en caféine ou en théophylline (café, boissons fraîches contenant de la caféine, thé).
Des interactions peuvent particulièrement exister avec les anesthésiants à l’oxyde azoteux (gaz hilarant). Si une opération est prévue, parlez-en à votre médecin.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par stylo pré-rempli, c’est-à-dire qu’il est essentiellement «sans sodium».
Veuillez informer votre médecin ou votre pharmacien si :
– vous souffrez d’une autre maladie,
– vous êtes allergique,
– vous prenez déjà d’autres médicaments en usage interne ou externe (même en automédication)!
METOJECT AUTO-INJECTEUR peut-il être utilisé pendant la grossesse ou l’allaitement ?
Grossesse
N’utilisez pas Metoject Auto-injecteur pendant la grossesse ou si vous essayez de tomber enceinte. Le méthotrexate peut provoquer des malformations congénitales, avoir des effets nocifs sur l’enfant à naître ou provoquer des fausses couches. Il est associé à des malformations du crâne, du visage, du cœur et des vaisseaux sanguins, du cerveau et des membres. Il est dès lors très important de ne pas administrer de méthotrexate aux patientes enceintes ou à celles qui envisagent de le devenir. Chez les femmes en âge de procréer, toute possibilité de grossesse doit être exclue en prenant des mesures appropriées (test de grossesse) avant le début du traitement.
Vous devez éviter de tomber enceinte pendant le traitement par le méthotrexate et pendant au moins 6 mois après l’arrêt du traitement en utilisant une contraception fiable durant toute cette période.
Si vous tombez enceinte au cours du traitement ou si vous pensez l’être, consultez votre médecin dès que possible. Une information médicale sur les risques d’effets nocifs du traitement sur l’enfant doit vous être fournie. Si vous souhaitez tomber enceinte, vous devez consulter votre médecin, qui pourra vous adresser à un spécialiste avant le début planifié du traitement.
Allaitement
N’allaitez pas pendant le traitement, car le méthotrexate passe dans le lait maternel. Si votre médecin considère qu’un traitement par le méthotrexate est absolument nécessaire pendant la période d’allaitement, vous devez arrêter d’allaiter.
Fertilité masculine
Les éléments de preuve disponibles n’indiquent pas une augmentation du risque de malformations ou de fausse couche si le père prend du méthotrexate à une dose inférieure à 30 mg/semaine. Il n’est néanmoins pas possible d’exclure totalement ce risque. Le méthotrexate peut être génotoxique et peut affecter la production des spermatozoïdes avec la possibilité de provoquer des anomalies congénitales. Vous devez éviter de concevoir un enfant ou de donner du sperme pendant le traitement par le méthotrexate et pendant au moins 3 mois après l’arrêt du traitement.
Comment utiliser METOJECT AUTO-INJECTEUR ?
Veuillez-vous conformer exactement aux indications de votre médecin lors de l’utilisation de Metoject Auto-injecteur. Veuillez-vous adresser à votre médecin ou à votre pharmacien en cas doute.
Le médecin qui vous prescrit Metoject Auto-injecteur doit être familiarisé avec l’activité du médicament et avec ses effets secondaires.
Au début du traitement, Metoject est injecté par le personnel médical. Avec l’accord de votre médecin, vous pouvez également apprendre à vous injecter vous-même Metoject. Dans ce cas, vous recevrez des instructions appropriées. Vous ne devez en aucun cas vous administrer vous-même une injection si vous n’avez pas encore appris à le faire.
Metoject Auto-injecteur n’est utilisé qu’une fois par semaine. Il est recommandé de réserver un jour spécifique et approprié pour l’injection (jour Metoject) et de maintenir ce même jour si possible pendant toute la durée du traitement.
Posologie chez l’adulte avec une arthrite rhumatoïde:
La dose initiale recommandée est de 7,5 mg de méthotrexate une fois par semaine en une seule injection Cette dose peut être augmentée par paliers de 2,5 mg/semaine, jusqu’à l’obtention d’un résultat optimal. De manière générale, ne pas dépasser une dose hebdomadaire de 25 mg.
Posologie chez les patients avec un psoriasis vulgaire et un psoriasis arthropathique:
Une semaine avant le début du traitement vous allez recevoir une dose test de 5 – 10 mg, afin d’éprouver votre tolérance. La dose initiale recommandée est de 7,5 mg de méthotrexate une fois par semaine en une seule injection. Cette dose peut être augmentée progressivement jusqu’à l’obtention d’un résultat optimal. Toutefois, une dose maximale de 25 mg de méthotrexate par une semaine ne devrait pas être dépassée. Dans des cas exceptionnels, le médecin peut prescrire une dose hebdomadaire de 30 mg.
Posologie chez les patients adultes atteints d’une maladie de Crohn:
La dose initiale recommandée est de 25 mg de méthotrexate une fois par semaine. Une période de 8 à 12 semaines peut s’écouler avant d’observer une réponse indiquant le succès du traitement. Pendant le traitement d’entretien, la dose généralement utilisée est de 15 mg de méthotrexate une fois par semaine.
Patients avec une insuffisance rénale:
Les patients avec une légère insuffisance rénale (clairance de la créatinine de 30 – 59 ml/min) devraient recevoir 50 % de la dose normale. Lors d’insuffisance rénale grave (clairance de la créatinine < 30 ml/min), le méthotrexate ne doit pas être utilisé.
Patients avec une insuffisance hépatique:
Les patients avec une insuffisance hépatique ne doivent utiliser Metoject Auto-injecteur qu’avec la plus grande prudence. Si le taux de bilirubine est >5 mg/dl, le méthotrexate ne doit pas être utilisé.
Utilisation chez le patient âgé:
Chez les patients âgés, le médecin peut envisager une réduction du dosage.
Utilisation chez les enfants et les adolescents:
La dose recommandée est de 10 – 15 mg/m² de surface corporelle par semaine. Lors d’inefficacité du traitement, la dose peut être augmentée jusqu’à 20 mg/m² de surface corporelle. Avec une insuffisance rénale (clairance de la créatinine <80 ml/min), Metoject Auto-injecteur ne doit pas être utilisé.
Metoject Auto-injecteur est injecté par voie sous-cutanée (dans le tissu sous-cutané).
Lorsque le méthotrexate entre accidentellement en contact avec votre peau ou avec vos muqueuses, les zones concernées seront immédiatement lavées à grande eau.
Les stylos pré-remplis sont destinées à un usage unique. Toute solution entamée sera jetée.
Lorsque vous avez oublié d’utiliser Metoject Auto-injecteur, ne doublez pas la dose, mais demandez conseil à votre médecin sans délai.
Lorsqu’il existe un doute de surdosage avec Metoject Auto-injecteur, veuillez en informer immédiatement votre médecin. En fonction de la gravité de vos symptômes, il décidera des mesures nécessaires.
Votre médecin décide de la durée de votre traitement. Lors d’arthrite rhumatoïde, la réponse au traitement pourra prendre environ 4 à 8 semaines. Dès que l’efficacité thérapeutique est atteinte, votre médecin réduira votre traitement progressivement à la dose d’entretien minimale efficace.
Lors de psoriasis vulgaire et de psoriasis arthropathique, il faudra compter avec une réponse au traitement après un délai d’environ 2 à 6 semaines. Dès que l’efficacité thérapeutique est atteinte, votre médecin réduira votre traitement progressivement à la dose d’entretien minimale efficace.
Ne changez pas le dosage prescrit de votre propre chef. Adressez-vous à votre médecin ou à votre pharmacien lorsque vous estimez que l’efficacité de votre médicament est trop faible ou au contraire trop forte.
Quels effets secondaires METOJECT AUTO-INJECTEUR peut-il provoquer ?
La survenue et la gravité des effets secondaires dépendent du dosage et de la fréquence d’utilisation. Des effets secondaires graves peuvent survenir même lors de dosages faibles, il est donc indispensable que votre médecin procède chez vous à des contrôles réguliers à intervalles rapprochés.
L’utilisation de Metoject Auto-injecteur peut provoquer les effets secondaires suivants:
Les effets secondaires apparaissant le plus fréquemment sont des troubles de système sanguin (ou système hématopoïétique) et des troubles gastro-intestinaux:
Lors de l’évaluation des effets secondaires, les paramètres de fréquence suivants sont utilisés:
Très fréquent: concerne plus d’un utilisateur sur 10
Fréquent: concerne 1 à 10 utilisateurs sur 100
Occasionnel: concerne 1 à 10 utilisateurs sur 1000
Rare: concerne 1 à 10 utilisateurs sur 10 000
Très rare: concerne moins d’un utilisateur sur 10 000, y compris cas isolés
Fréquence inconnue: ne peut être estimée sur la base des données disponibles
Affections gastro-intestinales:
Très fréquent: inflammation de la bouche (stomatite), troubles digestifs, nausées, perte d’appétit.
Fréquent: ulcères dans la région de la bouche et du pharynx, diarrhées.
Occasionnel: inflammation dans le région pharyngée, inflammation intestinale, pancréatite, vomissements.
Rare: ulcères du tractus gastro-intestinal.
Très rare: vomissements de sang (hématémèse), saignements importants.
Affections de la peau et du tissu sous-cutané:
Fréquent: éruption cutanée (exanthème), rougeur de la peau (érythème), démangeaisons (prurit).
Occasionnel: sensibilité accrue de la peau à l’exposition solaire (photosensibilité), chute de cheveux, augmentation des nodules rhumatismaux, zona (herpes zoster), inflammation des vaisseaux sanguins (vasculite), éruption cutanée herpétiforme, éruption cutanée prurigineuse (urticaire).
Rare: pigmentation accrue de la peau.
Très rare: réaction cutanée allergique à risque létal, accompagnée de fièvre et de vésicules (syndrome de Stevens-Johnson), nécrolyse épidermique toxique (décollement bulleux de l’épiderme, syndrome de Lyell), pigmentation accrue des ongles, panaris (paronychie aiguë).
Fréquence inconnue: rougeur et desquamation de la peau.
Troubles généraux et anomalies au site d’administration:
Rare: réactions d’hypersensibilité (réactions allergiques), choc allergique (anaphylactique), inflammation vasculaire de type allergique (vasculite), fière, yeux rouges (conjonctivite), infections, infection du sang (septicémie), guérison retardée des plaies, accumulation de liquide autour des poumons (épanchement pleural), accumulation de liquide entre les feuillets du cœur (épanchement péricardique), entrave au remplissage des chambres cardiaques (tamponnade péricardique), diminution des anticorps dans le sang (hypogammaglobulinémie).
Lors d’injection intramusculaire, il est possible d’observer des effets indésirables au niveau du site d’injection (sensation de brûlure) ou des troubles tissulaires (formation d’abcès stériles, atrophie du tissu graisseux).
Fréquence inconnue: gonflement.
Affections du système nerveux:
Fréquent: maux de tête, fatigue, somnolence.
Occasionnel: vertiges, confusion, dépression (fort sentiment de tristesse).
Très rare: troubles de la vue, douleurs, faiblesse musculaire ou sensations anormales telles qu’engourdissement ou picotements / moins de sensation au toucher que d’habitude, goût métallique dans la bouche, crampes, signes de méningite sans inflammation, paralysie (perte de la fonction musculaire).
Fréquence inconnue: encéphalopathie / leucoencéphalopathie.
Affections hépatobiliaires:
Très fréquent: augmentation du taux sanguin des enzymes hépatiques (transaminases).
Occasionnel: cirrhose du foie (dégénération conjonctive, respectivement fibreuse du tissu du foie), fibrose hépatique (transformation cicatricielle), dégénérescence graisseuse du foie.
Affections respiratoires, thoraciques et médiastinales:
Fréquent: inflammation de type allergique du squelette et des alvéoles (pneumonie interstitielle/alvéolite). Les premiers signes sont : une toux sèche irritative, un essoufflement (dyspnée) jusqu’à l’étouffement et de la fièvre.
Rares: fibrose pulmonaire (transformation cicatricielle des poumons), inflammation pulmonaire causée par des agents infectieux tels que Pneumocystis-Carinii, dyspnée, essoufflement (dyspnée) jusqu’à l’étouffement et asthme bronchique.
Fréquence inconnue: saignement des poumons.
Affections hématologiques et du système lymphatique:
Fréquent: altération de la formation des cellules sanguines avec une diminution pathologique des globules blancs et/ou rouges et/ou des plaquettes sanguines (leucopénie, anémie, thrombocytopénie).
Occasionnel: chute massive des globules et des plaquettes sanguines (pancytopénie).
Très rare: chute massive des globules blancs (agranulocytose), insuffisance médullaire grave.
Affections du rein et des voies urinaires:
Occasionnel: Inflammations et ulcères dans la région vésicale, insuffisance rénale, troubles mictionnels.
Rare: Insuffisance rénale, diminution ou réduction massive de l’excrétion urinaire, troubles électrolytiques.
Affections des organes de reproduction et du sein:
Occasionnel: Inflammations et ulcères dans la région vaginale.
Très rare: perte de l’appétit sexuel, impuissance, troubles de la formation du sperme (cellules germinales masculines), troubles du cycle menstruel et des règles, écoulement vaginal.
Affections musculosquelettiques et du tissu conjonctif:
Occasionnel: douleurs articulaires, douleurs musculaires, diminution de la masse osseuse (ostéoporose).
Tumeurs bénignes, malignes et non précisées (incl kystes et polypes):
Très rare: dans de rares cas, une tuméfaction des ganglions lymphatiques a été signalée (lymphomes). Cette tuméfaction a régressé spontanément après l’arrêt du traitement par méthotrexate dans quelques cas. Une augmentation des lymphomes sous méthotrexate n’a à l’heure actuelle pas été confirmée.
Si vous remarquez des effets secondaires qui ne sont pas décrits ici, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Metoject Auto-injecteur doit être conservé à température ambiante (15 – 25 °C). Conserver le produit dans son emballage d’origine à l’abri de la lumière.
Metoject Auto-injecteur est à conserver hors de la portée des enfants.
Remarques complémentaires
Les femmes enceintes du personnel médical ne doivent ni manipuler ni administrer Metoject Auto-injecteur.
Le méthotrexate ne doit pas entrer en contact avec votre peau ou vos muqueuses. En cas de contamination, les zones concernées seront immédiatement lavées à grande eau.
Médicament à usage unique. Toute solution entamée sera jetée.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien qui dispose d’une information détaillée destinée aux professionnels.
Que contient METOJECT AUTO-INJECTEUR ?
Principes actifs
1 ml de Metoject Auto-injecteur contient 50 mg de principe actif méthotrexate (sous la forme de méthotrexate-disodique).
Excipients
1 ml de Metoject Auto-injecteur contient en tant qu’excipients chlorure de sodium, hydroxyde de sodium, acide chlorhydrique, et de l’eau pour préparations injectables.
Numéro d’autorisation
65672 (Swissmedic)
Où obtenez-vous METOJECT AUTO-INJECTEUR ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, seulement sur ordonnance médicale non renouvelable.
Auto-injecteur à 7,5 mg (0,15 ml), 10 mg (0,2 ml), 12.5 mg (0,25 ml),15 mg (0,3 ml), 17,5 mg (0,35 ml), 20 mg (0,4 ml), 22,5 mg (0,45 ml), 25 mg (0,5 ml), 27,5 mg (0,55 ml) et 30 mg (0,6 ml).
Disponible dans des emballages à 1, 4, 6, 12 ou 24 auto-injecteurs.
À usage sous-cutané.
Titulaire de l’autorisation
Gebro Pharma AG, 4410 Liestal
Cette notice d’emballage a été vérifiée pour la dernière fois en juin 2023 par l’autorité de contrôle des médicaments (Swissmedic).
Remarques concertant l’utilisation
Recommandations
Lisez attentivement les suivantes instructions avant de commencer l’injection. Utilisez toujours exactement la technique d’injection que votre médecin ou votre pharmacien vous a montrée.
Information complémentaire
Les prescriptions nationales en vigueur doivent être respectées lors de la manipulation et de l’élimination du médicament et de la seringue prête à l’emploi. Les femmes enceintes appartenant au personnel médical ne doivent pas manipuler et/ou administrer Metoject Auto-injecteur.
Le méthotrexate ne doit pas entrer en contact avec la surface de la peau ou les muqueuses. Si cela s’est néanmoins produit, les zones touchées doivent immédiatement être rincées abondamment à l’eau.
Matériel nécessaire pour l’administration d’une injection avec l’auto-injecteur Metoject
Il vous faut:
• 1 auto-injecteur de Metoject Auto-injecteur
• 1 tampon imbibé d’alcool
Composants de l’auto-injecteur Metoject Auto-injecteur:
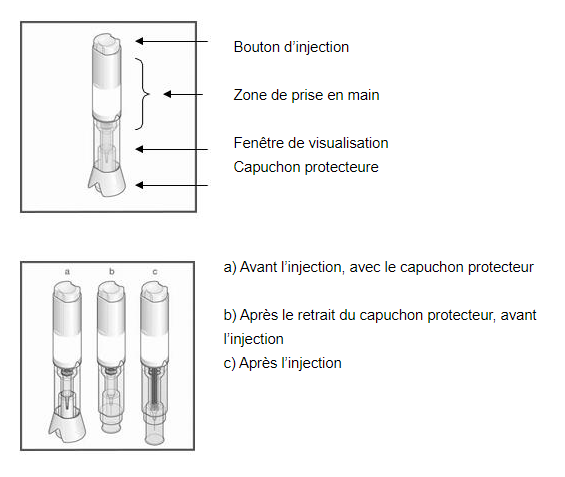
Ce que vous devez faire avant l’injection
1. Lavez-vous soigneusement les mains.
2. Sortez le système de l’emballage.
3. Avant l’utilisation, vérifiez que l’auto-injecteur ne présente pas de dommages visibles (ou de fissures).

4. Posez l’auto-injecteur Metoject Auto-injecteur sur une surface lisse et propre (p. ex. une table).
Quel site faut-il choisir pour l’injection
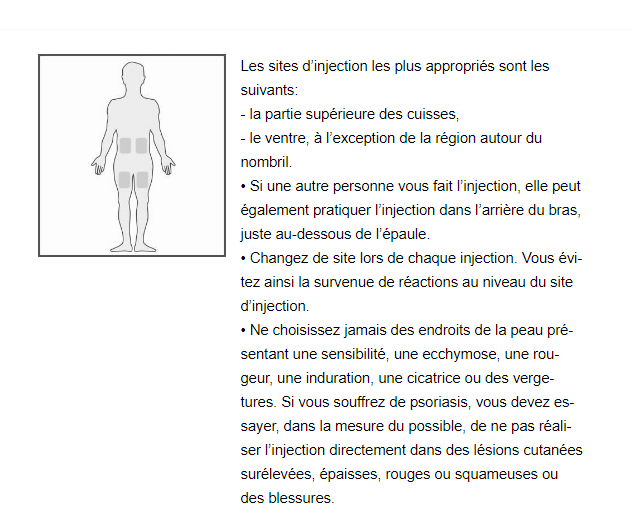
Comment préparer l’injection
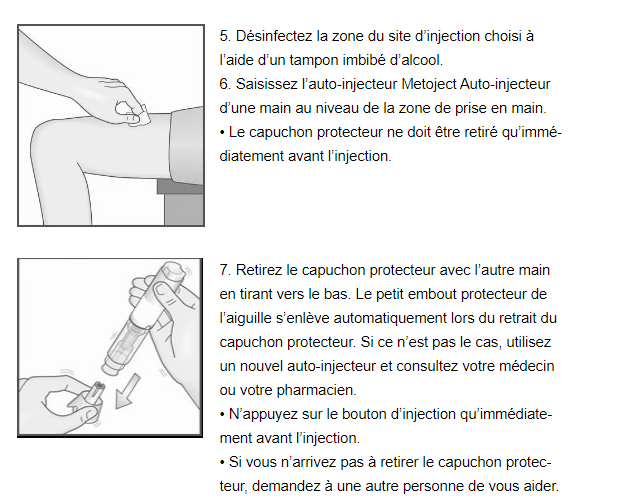
Remarque: l’injection doit être réalisée sans délai après le retrait du capuchon protecteur.
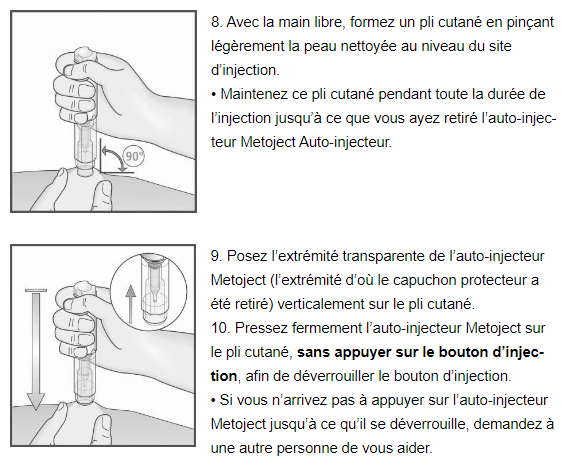
Comment procéder à l’injection:

Remarque:
Ne retirez pas prématurément l’auto-injecteur Metoject de la peau pour éviter que l’injection ne soit incomplète.
Si l’injection ne s’est pas déclenchée, relâchez le bouton d’injection. Vérifiez que l’auto-injecteur Metoject est fermement maintenu contre la peau et appuyez de nouveau fermement sur le bouton d’injection.
Si vous avez des troubles de l’audition, compter jusqu’à 5 après avoir appuyé sur le bouton d’injection. Soulevez ensuite l’auto-injecteur Metoject du site d’injection.
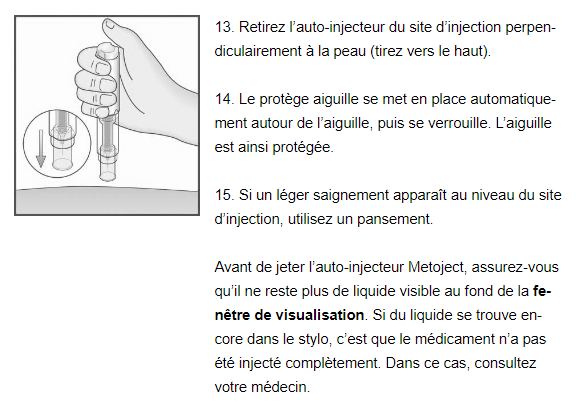
Remarque
Afin de prévenir toute blessure, vous ne devez jamais mettre les doigts dans l’orifice du protège aiguille situé au-dessus de l’aiguille. Ne pas casser le stylo.
À qui s’adresser en cas de problèmes
ð Adressez-vous à votre médecin ou à votre pharmacien pour tout problème ou question. ð Si vous ou une autre personne vous blessez avec l’aiguille, consultez immédiatement votre médecin et jetez l’auto-injecteur Metoject
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 25.09.2023, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans un paragraphe en gras ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 2ème mise à jour de cette page depuis le lancement début 2021 de cette rubrique. Mise à jour 1 (Décembre 2021 )
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


