Lenalidomid Zentiva®
Information destinée aux patients en Suisse
Qu’est-ce que le Lenalidomid Zentiva et quand doit-il être utilisé ?
Sur prescription du médecin.
Lenalidomid Zentiva contient l’agent actif le lénalidomide. Celui-ci influence certaines cellules et substances du système immunitaire et inhibe ainsi la formation de cellules sanguines cancéreuses.
Lenalidomid Zentiva est administré seul ou en association avec d’autres médicaments chez les patients souffrant d’un myélome multiple (un cancer caractérisé par la prolifération massive de certaines cellules dans la moelle osseuse).
Lenalidomid Zentiva en monothérapie est instauré pour traiter les patients adultes souffrant d’un myélome multiple, chez qui une greffe de moelle osseuse a été réalisée.
Lenalidomid Zentiva est instauré en association avec le bortézomib (appelé un inhibiteur du protéasome) et la dexaméthasone (un médicament anti-inflammatoire) pour le traitement des patients adultes chez qui un myélome multiple a été récemment diagnostiqué.
Pour les patients chez qui un myélome multiple a été récemment diagnostiqué et qui ne peuvent pas recevoir une greffe de moelle osseuse, il existe deux types de traitement:
– Le premier type de traitement consiste à administrer Lenalidomid Zentiva en association avec un médicament anti-inflammatoire appelé «dexaméthasone».
– Le second type de traitement consiste à administrer Lenalidomid Zentiva en association avec un médicament de chimiothérapie appelé «melphalan» et avec un médicament qui agit comme un suppresseur du système immunitaire appelé «prednisone». Vous prendrez ces autres médicaments en association avec Lenalidomid Zentiva au début du traitement et vous continuerez ensuite en prenant Lenalidomid Zentiva seul.
Chez les patients atteints de myélome multiple, ayant reçu au moins une autre forme de traitement pour leur maladie, Lenalidomid Zentiva est pris en association avec un médicament anti-inflammatoire appelé «dexaméthasone».
Lenalidomid Zentiva est utilisé seul dans le traitement des patients et des patientes adultes chez lesquels certains types de syndromes myélodysplasiques ont été diagnostiqués. Chez les patients et les patientes atteints de syndrome myélodysplasique, la moelle osseuse ne fabrique pas suffisamment de cellules sanguines saines dans le corps. Lenalidomid Zentiva est utilisé dans certains types de syndrome myélodysplasique, lorsque les patients et les patientes ont moins de globules rouges que la normale, lorsqu’ils/elles doivent recevoir des transfusions sanguines et présentent par ailleurs une certaine modification chromosomique.
Lenalidomid Zentiva est utilisé seul chez les patients qui présentent un lymphome à cellules du manteau récidivant (un type de cancer particulier du système lymphatique) déjà traités précédemment par le bortezomib et une chimiothérapie associée au rituximab.
Lenalidomid Zentiva est pris en association avec le rituximab pour le traitement des patients adultes atteints de lymphome folliculaire (LF) préalablement traité, dont la maladie a réapparu ou ne s’est pas améliorée après un ou plusieurs traitements antérieurs. Le LF est un cancer à progression lente qui touche les lymphocytes B, un type de globules blancs qui aident l’organisme à lutter contre les infections. En cas de LF, un nombre excessif de ces lymphocytes B malades peuvent s’accumuler dans le sang, la moelle osseuse, les ganglions lymphatiques et la rate et finissent par remplacer les cellules saines.
Quand Lenalidomid Zentiva ne doit-il pas être pris ?
Si vous êtes enceinte, si vous pensez être enceinte ou si vous prévoyez de l’être.
Chez les femmes en âge de procréer, sauf si une méthode de contraception très fiable est rigoureusement appliquée; voir également la section «Quelles sont les précautions à observer lors de l’utilisation de Lenalidomid Zentiva ?».
Lors d’une hypersensibilité (allergie) à la substance active lénalidomide ou à l’un des excipients.
Quelles sont les précautions à observer lors de la prise de Lenalidomid Zentiva ?
Contraception
Dans des cas particuliers, le médecin peut prescrire Lenalidomid Zentiva à des femmes en âge de procréer. Si tel est le cas chez vous, il est absolument impératif que vous suiviez à la lettre les directives de votre médecin. Les points suivants sont très importants:
1.Avant le début du traitement, votre médecin vérifiera que vous n’êtes pas enceinte. Par la suite, il vous soumettra à un test de grossesse toutes les 4 semaines pendant toute la durée du traitement, ainsi qu’à un dernier test de grossesse 4 semaines après la fin du traitement.
2.Votre médecin ou un autre médecin vous conseillera au sujet des méthodes de contraception appropriées dans votre cas. Vous devez généralement commencer à appliquer ces méthodes 4 semaines avant le début du traitement, et en poursuivre strictement l’application non seulement pendant toute la durée du traitement, pauses de traitement comprises, mais encore pendant les quatre semaines qui suivront le traitement.
3.Si vous êtes enceinte ou si vous pensez que vous pourriez l’être malgré l’application consciencieuse des mesures de contraception pendant votre traitement par Lenalidomid Zentiva ou au cours des quatre semaines suivant le traitement, vous devez immédiatement en avertir votre médecin. Celui-ci initiera alors les mesures nécessaires.
Les patients de sexe masculin qui ont des rapports sexuels avec une femme en âge de procréer doivent utiliser des préservatifs pendant toute la durée du traitement, pauses de traitement comprises, et pendant les 7 jours suivant la fin du traitement. En outre, les patients ne doivent en aucun cas faire un don de sperme pendant leur traitement par le lénalidomide ou pendant les 7 jours suivant la fin de ce traitement.
En raison du risque pour l’enfant à naître, vous ne devez jamais remettre Lenalidomid Zentiva à une autre personne.
Vous ne devez pas donner votre sang pendant le traitement, pendant ses interruptions ni pendant au moins 7 jours après l’arrêt du traitement.
Le titulaire de l’autorisation de Lenalidomid Zentiva met les matériels suivants à votre disposition:
– Information sur les problèmes associés à une grossesse sous Lenalidomid Zentiva.
– Un formulaire que vous devez signer pour confirmer que vous avez bien compris la nécessité d’empêcher une grossesse pendant un traitement par Lenalidomid Zentiva.
Autres précautions
Votre médecin fera régulièrement des analyses de votre sang au cours de votre traitement par Lenalidomid Zentiva parce que ce traitement peut provoquer une réduction des nombres de globules blancs, de globules rouges et de plaquettes sanguines. Ces réductions peuvent entraîner une prédisposition accrue aux infections et aux complications hémorragiques. Par conséquent, vous devez prévenir votre médecin sans tarder si vous avez des hémorragies et/ou des ecchymoses (p.ex. saignement de nez ou hématomes), ou encore si vous constatez l’apparition d’une fièvre, d’un mal de gorge, d’ulcérations dans la bouche ou d’autres signes d’une infection.
Votre médecin contrôlera aussi la fonction de votre glande thyroïde au cours du traitement par Lenalidomid Zentiva, étant donné qu’une augmentation ou une réduction de la fonction thyroïdienne peut se développer.
Ensuite, votre médecin vous surveillera pour vérifier la présence éventuelle d’une réaction de flambée tumorale. Il s’agit d’une aggravation temporaire des symptômes liés à la tumeur. Des symptômes comme un gonflement douloureux des ganglions lymphatiques, une température sub-fébrile, des douleurs et des éruptions cutanées peuvent survenir après une réaction de flambée tumorale. Des décès ont également été signalés.
Des cas de syndrome de lyse tumorale (dont certains ont entraîné le décès) ont été observés à la suite de la destruction rapide des cellules tumorales, surtout chez les patients atteints d’un lymphome à cellules du manteau et présentant un nombre élevé de lymphocytes avant le début du traitement par Lenalidomid Zentiva.
Adressez-vous à votre médecin si vous observez des symptômes comme nausée, essoufflement, battements du cœur irréguliers, urine trouble, fatigue et/ou troubles articulaires.
Vous pouvez subir des examens pour détecter des signes de problèmes cardiopulmonaires avant et pendant le traitement par lénalidomide. Dans ce cas, votre médecin contrôlera éventuellement votre fonctions cardiaques par ECG, en particulier si vous utilisez simultanément un médicament qui influence les fonctions du cœur ou si vous souffrez d’un certain trouble cardiaque nommé syndrome du QT long. Consultez votre médecin si vous avez des douleurs dans la poitrine qui irradient dans le bras, le cou, la mâchoire, le dos ou l’estomac et si vous avez des sueurs, des difficultés respiratoires, des nausées ou vomissements. Ils peuvent être les symptômes d’un infarctus du myocarde.
Votre médecin surveillera la concentration de digoxine dans le sang lorsque vous prenez des médicaments pour le cœur contenant comme principe actif la digoxine pendant le traitement par Lenalidomid Zentiva.
Pendant le traitement par Lenalidomid Zentiva, le risque de développer des caillots sanguins dans les vaisseaux sanguins, à type de thromboses artérielles (par exemple un infarctus du myocarde ou un accident vasculaire cérébral) et d’événements thrombo-emboliques veineux (par exemple une thrombose veineuse ou une embolie pulmonaire), est accru. Vous devez prévenir votre médecin sans attendre si vous observez les signes d’une thrombose, par exemple douleurs et/ou gonflement d’un membre inférieur ou supérieur, douleurs dans la poitrine, toux ou troubles respiratoires soudains. En raison du risque accru de thromboses, il convient d’éviter tout traitement hormonal substitutif postménopausique et tout traitement à base de préparations d’érythropoïétines (médicaments qui stimulent la formation de globules rouges).
Informez immédiatement votre médecin ou le personnel médical si l’un des symptômes suivants survient pendant ou après le traitement:
essoufflement, fatigue, vertiges, douleur dans la poitrine, accélération des battements du cœur ou gonflement dans les jambes ou les chevilles. Il peut s’agir de signes d’une maladie grave appelée hypertension pulmonaire.
Pendant le traitement par Lenalidomid Zentiva, une détérioration de la fonction hépatique peut survenir, pouvant aller jusqu’à une lésion hépatique. Veuillez informer votre médecin si vous avez souffert ou souffrez de problèmes hépatiques, si l’on sait déjà que votre fonction rénale est insuffisante ou si vous prenez des médicaments, en particulier des antibiotiques, car ces circonstances peuvent augmenter le risque d’un trouble hépatique.
Dans certains cas, une réaction de rejet de la greffe est survenue chez les receveurs de greffe d’organe après le traitement par Lenalidomid Zentiva. Si vous subissez une greffe d’organe, votre médecin surveillera chez vous des réactions de rejet.
Des réactions allergiques graves éventuelles (appelées angiœdème et anaphylaxie) peuvent se manifester sous forme d’urticaire, d’éruption cutanée, de gonflement des yeux, de la bouche ou du visage, d’essoufflement ou de démangeaisons. Dans le cas de réactions allergiques sévères, des éruptions cutanées peuvent survenir, qui, au début, sont délimitées mais ensuite s’étendent sur tout le corps et sont accompagnées de desquamations importantes (appelées syndrome de Stevens-Johnson et/ou nécrolyse épidermique toxique). Dans des cas très rares, outre les réactions cutanées, les réactions allergiques peuvent être accompagnées de fièvre, fatigue, gonflement des ganglions lymphatiques, d’une augmentation de certains globules blancs (éosinophilie) ainsi que d’effets sur le foie, les reins ou les poumons (appelées DRESS). Ces réactions allergiques peuvent avoir une issue fatale. Vous devez immédiatement informer votre médecin si vous développez de tels symptômes.
Par son action inhibitrice sur le système immunitaire, Lenalidomid Zentiva peut entraîner une inefficacité de certains vaccins ou un risque d’infection lors d’une administration de vaccins vivants. Vous devrez donc renoncer aux vaccinations pendant le traitement par Lenalidomid Zentiva.
La prudence est de mise lors d’une utilisation concomitante de Lenalidomid Zentiva et d’autres médicaments immunomodulateurs. Les médicaments inhibiteurs de la coagulation doivent être utilisés avec Lenalidomid Zentiva uniquement après en avoir discuté avec votre médecin.
Par conséquent, vous devez informer votre médecin si vous utilisez déjà d’autres médicaments.
En raison d’effets indésirables possibles tels que somnolence, fatigue et vue trouble, vous devez user d’une prudence particulière pour conduire un véhicule ou utiliser une machine.
Il est important de savoir que d’autres types de cancers peuvent survenir chez un petit nombre de patients présentant un myélome multiple ou un lymphome des cellules du manteau et ce risque pourrait s’accroître lors d’un traitement par Lenalidomid Zentiva. C’est pourquoi votre médecin entreprendra une évaluation soigneuse du rapport bénéfice-risque avant de prescrire Lenalidomid Zentiva.
Les patients atteints d’un myélome multiple ont tendance à développer des infections, dont des pneumonies. Un traitement par Lenalidomid Zentiva en association avec la dexaméthasone peut accroître cette vulnérabilité aux infections. Votre médecin vous surveillera à ce sujet et vous demandera de le consulter sans tarder au premier signe d’infection comme une toux ou une fièvre.
Chez les patients en mauvais état général, on a plutôt tendance à retrouver des problèmes de toxicité aux traitements par Lenalidomid Zentiva en association avec d’autres médicaments. Votre médecin évaluera de ce fait attentivement votre capacité à tolérer un traitement par Lenalidomid Zentiva en association, en tenant compte de votre âge et de votre état général.
De rares cas de réactivation de l’hépatite B ont été rapportés à la suite du traitement par Lenalidomid Zentiva chez des patients présentant des antécédents d’infection par le virus de l’hépatite B. C’est pourquoi, votre médecin vous surveillera étroitement pendant le traitement par Lenalidomid Zentiva afin de détecter les signes et symptômes d’une infection active par le virus de l’hépatite B. Veuillez informer votre médecin si vous avez des antécédents d’infection par le virus de l’hépatite B.
Veuillez informer votre médecin ou votre pharmacien si vous
– souffrez d’une autre maladie,
– si vous êtes allergique ou
– si vous prenez déjà d’autres médicaments en usage interne ou externe (même en automédication!).
Lactose
Lenalidomid Zentiva contient du lactose. Si votre médecin vous a informé(e) d’une intolérance à certains sucres, contactez-le avant de prendre ce médicament.
Sodium
Ce médicament renferme moins de 1 mmol de sodium (23 mg) par gélule, ce qui signifie qu’il s’agit d’un médicament pratiquement «sans sodium».
Lenalidomid Zentiva peut-il être pris pendant la grossesse ou l’allaitement ?
Lenalidomid Zentiva ne peut pas être utilisé pendant la grossesse.
Les femmes en âge de procréer doivent absolument éviter de débuter une grossesse pendant le traitement par Lenalidomid Zentiva. Pour exclure une grossesse, il faudra faire des tests de grossesse avant le traitement, pendant le traitement et à la fin du traitement et une méthode de contraception fiable devra être appliquée pendant et plusieurs semaines après le traitement par Lenalidomid Zentiva.
On ne sait pas si Lenalidomid Zentiva passe dans le lait maternel. Par conséquent, Lenalidomid Zentiva ne doit pas être utilisé pendant la période d’allaitement. Si une patiente qui allaite doit être traitée par Lenalidomid Zentiva, elle devra d’abord sevrer son bébé.
Le lénalidomide passe dans le sperme. Les patients de sexe masculin ayant une partenaire en âge de procréer devront toujours utiliser des préservatifs pendant le traitement par Lenalidomid Zentiva et pendant les 7 jours après l’arrêt du traitement.
Vous trouverez des informations détaillées sur la contraception à la section «Quelles sont les précautions à observer lors de l’utilisation de Lenalidomid Zentiva ?».
Comment utiliser Lenalidomid Zentiva ?
Prenez toujours Lenalidomid Zentiva exactement comme prescrit par le médecin. Questionnez votre médecin ou votre pharmacien si vous avez de quelconques incertitudes.
Les gélules Lenalidomid Zentiva doivent être prises avec un peu d’eau, au cours ou en dehors des repas, à peu près à heure fixe chaque jour. Elles ne doivent être ni ouvertes, ni croquées. Les mains doivent être lavées immédiatement après tout contact avec les gélules. Veillez à ne jamais aspirer la poudre contenue dans les gélules (par exemple à partir d’une gélule endommagée) et à éviter tout contact de la poudre avec la peau ou les muqueuses (yeux!). Si un contact avec la peau s’est néanmoins produit, lavez la partie du corps concernée à l’eau et au savon. Dans le cas d’un contact accidentel avec les yeux, rincez abondamment l’œil concerné à l’eau claire.
Pour sortir la gélule de la plaquette, appuyez seulement sur une extrémité de la gélule pour la pousser à travers la pellicule d’aluminium. N’exercez pas de pression sur le centre de la gélule, car cela peut provoquer sa rupture.
Posologie de Lenalidomid Zentiva en association avec le bortézomib et la dexaméthasone chez des patients atteints d’un myélome multiple non préalablement traité
La dose usuelle de Lenalidomid Zentiva est de 25 mg une fois par jour. Il existe deux schémas thérapeutiques différents, chacun en fonction des consignes de votre médecin:
a) Prenez Lenalidomid Zentiva 14 jours de suite, puis interrompez la prise de Lenalidomid Zentiva pour 7 jours. Un cycle de traitement dure donc 21 jours.
Ou
b) Prenez Lenalidomid Zentiva 21 jours de suite, puis interrompez la prise de Lenalidomid Zentiva pour 7 jours. Un cycle de traitement dure donc 28 jours. Votre médecin déterminera la dose de bortézomib, l’un des médicaments qui vous est administré en association avec Lenalidomid Zentiva, en fonction de votre poids et de votre taille.
Suivant les consignes de votre médecin, la dose de dexaméthasone, l’autre médicament que vous devez prendre en association avec Lenalidomid Zentiva, est de 20 mg une fois par jour, les jours 1, 2, 4, 5, 8, 9, 11, et 12 d’un cycle de traitement ou de 40 mg une fois par jour les jours 1 jusqu’à 4 et 9 jusqu’à 12 d’un cycle de traitement.
En fonction de l’évaluation faite par votre médecin, la posologie peut être adaptée individuellement.
Le schéma posologique usuel est décrit dans les tableaux suivants:
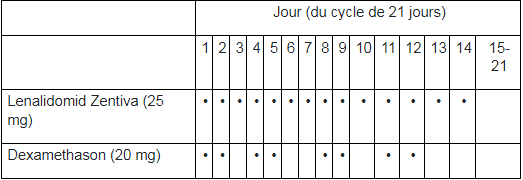
ou
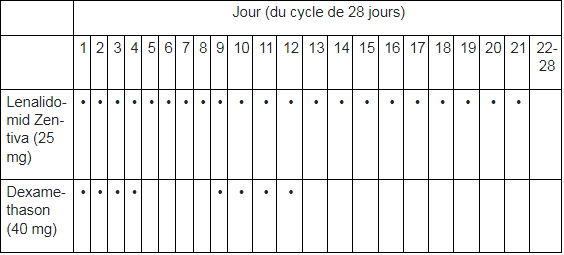
Posologie de Lenalidomid Zentiva chez des patients atteints d’un myélome multiple après une greffe de moelle osseuse
La dose usuelle de Lenalidomid Zentiva est de 10 mg en une prise par jour. En fonction de l’évaluation faite par votre médecin, cette posologie peut être augmentée à 15 mg en une prise par jour.
Posologie de Lenalidomid Zentiva en association avec la dexaméthasone chez les patients atteints d’un myélome multiple nouvellement diagnostiqué
La dose usuelle de Lenalidomid Zentiva est de 25 mg en une prise par jour. Prenez Lenalidomid Zentiva 21 jours de suite, puis interrompez la prise pour 7 jours. Un cycle de traitement dure donc 28 jours. La dose de dexaméthasone le médicament que vous devez prendre en association avec Lenalidomid Zentiva – est de 40 mg une fois par jour chez les patients de moins de 75 ans et de 20 mg une fois par jour chez les patients de plus de 75 ans. Vous prenez la dexaméthasone les jours 1, 8, 15 et 22 d’un cycle de traitement de 28 jours. En fonction de l’évaluation faite par votre médecin, cette posologie peut être adaptée individuellement.
Posologie de Lenalidomid Zentiva en association avec le melphalan et la prednisone chez les patients atteints d’un myélome multiple nouvellement diagnostiqué
La dose usuelle de Lenalidomid Zentiva est de 10 mg une fois par jour. Prenez Lenalidomid Zentiva 21 jours de suite, puis interrompez la prise pour 7 jours. Un cycle de traitement dure donc 28 jours. La dose de melphalan – le médicament que vous devez prendre en association avec Lenalidomid Zentiva – est de 0,18 mg/kg une fois par jour, les jours 1 à 4 d’un cycle de traitement de 28 jours. La dose de prednisone – le médicament que vous devez prendre en association avec Lenalidomid Zentiva – est de 2 mg/kg une fois par jour, les jours 1 à 4 d’un cycle de traitement de 28 jours.
Posologie de Lenalidomid Zentiva en association avec la dexaméthasone chez les patients atteints de myélome multiple ayant reçu au moins une autre forme de traitement pour leur maladie
La dose usuelle de Lenalidomid Zentiva est de 25 mg une fois par jour. Prenez Lenalidomid Zentiva 21 jours de suite, puis interrompez la prise pour 7 jours. Un cycle de traitement dure donc 28 jours.
La dose de dexaméthasone – le médicament que vous devez prendre en association avec Lenalidomid Zentiva – est de 40 mg une fois par jour. Le schéma posologique est généralement le suivant: pendant les quatre premiers cycles de traitement de 28 jours, vous prenez la dexaméthasone les jours 1 à 4, 9 à 12 et 17 à 20. Par la suite, vous ne prenez la dexaméthasone plus que les jours 1 à 4. En fonction de l’évaluation faite par votre médecin, cette posologie peut être adaptée individuellement.
Vous trouverez de plus amples informations sur la dexaméthasone dans la notice d’emballage de la préparation utilisée.
Posologie dans le syndrome myélodysplasique
La dose initiale recommandée est de 10 mg de Lenalidomid Zentiva une fois par jour du premier au 21e jour pendant les jours 1 à 21 de cycles consécutifs de 28 jours.
Posologie dans le lymphome des cellules du manteau
La dose initiale conseillée est de 25 mg de Lenalidomid Zentiva une fois par jour pendant les jours 1 à 21 de cycles consécutifs de 28 jours.
Posologie de Lenalidomid Zentiva en association avec le rituximab dans le lymphome folliculaire
La dose initiale recommandée est de 20 mg de Lenalidomid Zentiva en une prise par jour les jours 1 à 21 de chaque cycle de traitement de 28 jours. Votre médecin déterminera la dose de rituximab, l’un des médicaments qui vous est administré en association avec Lenalidomid Zentiva, en fonction de votre poids et de votre taille
Pendant le traitement par Lenalidomid Zentiva, votre médecin effectuera des analyses sanguines régulières, car une réduction des nombres de globules blancs et rouges ainsi que des plaquettes sanguines peut survenir. Si vos valeurs sanguines baissent fortement, votre médecin suspendra votre traitement par Lenalidomid Zentiva et le reprendra ensuite avec une plus faible dose.
Aucune étude sur l’utilisation de Lenalidomid Zentiva chez l’enfant ou l’adolescent n’est disponible. Par conséquent, Lenalidomid Zentiva n’est pas utilisé chez ces groupes de patients.
Chez les patients âgés, le médecin surveillera particulièrement attentivement le traitement.
Chez les patients souffrant d’un trouble fonctionnel des reins, le médecin surveillera particulièrement attentivement le traitement et mesurera plus fréquemment les valeurs de la fonction rénale.
Informez immédiatement votre médecin si vous avez pris Lenalidomid Zentiva en quantité plus importante que celle prescrite.
Si vous avez oublié une dose de Lenalidomid Zentiva et si l’heure de la prise oubliée remonte à moins de 12 heures, prenez immédiatement la gélule oubliée.
Si vous avez oublié une dose de Lenalidomid Zentiva et si l’heure de la prise oubliée remonte à plus de 12 heures, ne prenez plus la gélule oubliée. Attendez jusqu’au lendemain et prenez la prochaine gélule à l’heure habituelle.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Lenalidomid Zentiva peut-il provoquer ?
Très fréquents (concernent plus d’un utilisateur sur 10)
Inflammations du nez et de la gorge, bronchite, infections des voies urinaires, infection des voies respiratoires supérieures, inflammation des voies gastro-intestinales, pneumonie, inflammation de la muqueuse nasale, infections des sinus paranasaux, grippe, aggravation à court terme des symptômes liés à la tumeur (flambée tumorale), réduction des nombres de globules blancs, de globules rouges et de plaquettes sanguines, perte d’appétit, déshydratation, perte de poids, modifications des valeurs biologiques (notamment potassium, calcium, sodium, glycémie, résultats des tests de l’exploration fonctionnelle hépatique, enzymes), insomnies, perturbation du sens gustatif, céphalées (maux de tête), picotement, sensation d’engourdissement dans les membres, vertige, vue trouble, hypotension, toux, souffle court, diarrhée, constipation, nausées, douleurs abdominales, vomissement, sécheresse buccale ou lésions buccales, démangeaisons, exanthème (éruption cutanée), sécheresse cutanée, crampes ou faiblesse musculaires, douleurs dorsales, douleurs musculaires, douleurs dans la musculature squelettique, douleurs osseuses, épuisement, fièvre, œdèmes dans les bras et dans les jambes, manque d’énergie, dépression, cataracte, thrombose veineuse, troubles digestifs, douleurs articulaires, douleurs dans les membres, douleur dans la poitrine.
Fréquents (concernent 1 à 10 utilisateurs sur 100)
Infections localisées ou généralisées (causées par des bactéries, virus ou champignons, par exemple pneumonie, infection fongique dans la bouche), infections des voies respiratoires inférieures, infection pulmonaire, infections des voies respiratoires, infection du sang (septicémie), inflammation intestinale, inflammation du tissu sous-cutané, maladie du système hématopoïétique (leucémie myéloïde aiguë), maladies de la moelle osseuse (syndrome myélodysplasique), syndrome de lyse tumorale (complications métaboliques pouvant survenir pendant un traitement anti-cancéreux et parfois même en l’absence de traitement), tumeur de la peau, prise de poids, surcharge de fer, accumulation d’eau dans les tissus, anomalies hormonales (type cortisone, avec gonflement du visage et accumulation de graisse au niveau du torse), confusion mentale, changement de l’état d’humeur général, hallucinations visuelles ou auditives (voir des choses qui n’existent pas), fluctuations de l’humeur, anxiété/angoisse, irritabilité, fatigue, somnolence, troubles de la circulation cérébrale, évanouissement, sensations anormales ou faiblesse des membres, tremblements, troubles de la mémoire, névralgies, troubles de la vue, larmoiement, inflammation de la conjonctive (conjonctivite), rythme cardiaque accéléré ou irrégulier, hypertension artérielle (augmentation de la tension artérielle) ecchymoses, bouffées de chaleur, embolie pulmonaire, insuffisance respiratoire, écoulement nasal, inflammation de la gorge, hémorragie nasale, trouble de la voix, enrouement, hoquet, douleurs abdominales supérieures, ballonnements, peau rougie, gonflement du visage, coloration de la peau, transpiration, sueurs nocturnes, chute des cheveux, troubles de la fonction hépatique, lésions hépatiques, altération de la fonction rénale, troubles érectiles, agrandissement de la poitrine chez l’homme, règles anormales, chute, frissons, douleurs de la nuque, insuffisance rénale (aiguë), lésion rénale aiguë, douleurs thoraciques non cardiaques, contusion.
Occasionnels (concernent 1 à 10 utilisateurs sur 1000)
Inflammation de la paroi interne du cœur (endocardite), herpès ophtalmique, zona, infection auriculaire, maladie du système hématopoïétique (leucémie aiguë à lymphocytes T), prolongation du temps de coagulation, tuméfaction des ganglions, baisse de la fonction du cortex surrénalien, baisse de la fonction de la thyroïde, hyperactivité de la thyroïde, augmentation de la pilosité chez la femme, diabète, épuisement, goutte, augmentation de l’appétit, baisse de la libido, problèmes psychiatriques, nervosité, agressivité, cauchemars, attaque cérébrale (accident vasculaire cérébral), troubles de l’élocution, troubles du mouvement ou de l’équilibre, troubles de la concentration, perte de l’odorat, perte de l’acuité visuelle, inflammation cornéenne, irritation ou sécheresse des yeux, bourdonnements d’oreille, douleurs auriculaires, perte de l’audition, faiblesse cardiaque, ralentissement du pouls, collapsus cardiovasculaire, troubles de la circulation du sang, élévation de la pression artérielle dans les vaisseaux sanguins qui alimentent les poumons (hypertension artérielle pulmonaire), asthme, sang dans les matières vomies ou dans les selles (selles noirâtres), inflammation intestinale, troubles de la déglutition, hémorragies gingivales, hémorroïdes, eczéma, acné, hypersensibilité de la peau à la lumière, desquamation ou fissure de la peau, troubles osseux, raideur musculaire, tuméfaction articulaire, fréquent besoin d’uriner, incontinence urinaire, rétention urinaire, soif, sensation de froid, gonflement rapide de la peau, notamment au niveau du dos des mains ou des pieds, ou encore des paupières, des lèvres, du visage, de la langue ou des organes génitaux, réactivation du virus (virus de l’hépatite B, zona).
Rares (concernent 1 à 10 utilisateurs sur 10 000)
Réactions allergiques graves (anaphylaxie, syndrome de Stevens-Johnson ou nécrolyse épidermique toxique) inflammations du tissu pulmonaire, inflammations du pancréas, maladie aiguë du greffon contre l’hôte.
Très rares (concernent moins d’un utilisateur sur 10 000)
Réactions allergiques graves (éruption cutanée y compris éosinophilie et symptômes systémiques, appelée DRESS), maladie du cerveau causée par un virus (appelée leucoencéphalopathie multifocale progressive).
Fréquence indéterminée (ne peut être estimée à partir des données disponibles)
Rejet de greffe d’organe.
Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l’emballage.
Remarques concernant le stockage
Ne pas conserver au-dessus de 30°C, conserver dans l’emballage original et hors de portée des enfants.
Remarques complémentaires
Veillez à rapporter les gélules non utilisées ou endommagées à votre médecin ou à votre pharmacien pour que ces personnes en assurent l’élimination correcte.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien qui disposent d’une information détaillée destinée aux professionnels.
Que contient Lenalidomid Zentiva ?
Principes actifs
1 gélule Lenalidomid Zentiva contient 2,5 mg, 5 mg, 7,5 mg, 10 mg, 15 mg, 20 mg ou 25 mg lénalidomide comme principe actif.
Excipients
Cellulose microcristalline (E460), lactose anhydre, croscarmellose sodique (E468), stéarate de magnésium (E470b), gélatine, dioxyde de titane (E171), gommes laques (E904), propylèneglycol (E1520), oxyde de fer noir (E172), hydroxyde de potassium (E525).
Uniquement pour les gélules de 2,5 mg, 7,5 mg, 10 mg et 20 mg: oxyde de fer jaune (E172)
Uniquement pour les gélules de 2,5 mg, 10 mg, 15 mg et 20 mg: carmin indigo (E132)
Numéro d’autorisation
67850 (Swissmedic).
Où obtenez-vous Lenalidomid Zentiva ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale non renouvelable.
Lenalidomid Zentiva 2,5 mg, 5 mg, 7,5 mg, 10 mg, 15 mg, 20 mg, 25 mg: boîtes de 21 gélules
Titulaire de l’autorisation
Helvepharm AG, Frauenfeld
Cette notice d’emballage a été vérifiée pour la dernière fois en août 2022 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 22.02.2023, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 3ème mise à jour de cette page depuis le lancement début 2021 de cette rubrique. Mise à jour 1 (mars 2022). Mise à jour 2 (mai 2022).
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


