Konakion MM
Information destinée aux patients en Suisse
Qu’est-ce que le Konakion MM et quand est-il utilisé ?
Konakion MM contient comme principe actif de la vitamine K1 (phytoménadione), qui favorise la coagulation du sang. Votre médecin utilise Konakion MM pour traiter et prévenir des hémorragies consécutives à un manque de vitamine K, pour combattre une tendance aux hémorragies chez le nouveau-né ainsi que pour corriger un surdosage de certains produits s’opposant à la coagulation sanguine (anticoagulants).
Les ampoules de micelles mixtes de Konakion MM ne doivent être utilisées que sur prescription du médecin.
De quoi faut-il tenir compte en dehors du traitement ?
Si vous suivez un traitement par des produits destinés à fluidifier le sang, vous ne devez prendre ou utiliser Konakion MM que sur prescription du médecin et en vous conformant strictement à ses directives.
Quand Konakion MM ne doit-il pas être pris ?
Si vous êtes allergique (c.-à-d. si vous avez une hypersensibilité) au principe actif de Konakion MM ou à l’un de ses composants, vous ne devez pas utiliser ce produit (voir «Que contient Konakion MM ?»).
Quelles sont les précautions à observer lors de la prise de Konakion MM ?
Au moment de l’utilisation, la solution micellaire mixte se trouvant dans l’ampoule doit être limpide.
Les médicaments contre les convulsions (épilepsie) ainsi que ceux s’opposant à la coagulation du sang (fluidifiants sanguins) atténuent l’effet de Konakion MM.
Si vous souffrez de troubles sévères de la fonction hépatique, la coagulation de votre sang peut être altérée. Votre médecin surveillera la coagulation de votre sang par des examens de laboratoire.
Veuillez informer votre médecin ou votre pharmacien si vous souffrez d’une autre maladie, vous êtes allergique ou vous prenez ou utilisez déjà d’autres médicaments en usage externe (même en automédication!).
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule, c.-à-d. qu’il est essentiellement sans «sodium».
Konakion MM peut-il être pris pendant la grossesse ou l’allaitement ?
Pendant la grossesse et l’allaitement, Konakion MM peut être pris/utilisé dans les quantités prescrites par le médecin.
Comment utiliser Konakion MM ?
En cas d’hémorragies sévères ou mettant la vie du patient en danger
Dans ces cas Konakion MM est administré par le médecin lui-même, généralement sous forme d’une injection unique.
Chez le nouveau-né et le nourrisson de moins d’un an, il convient d’avoir recours au Konakion MM paediatric en raison du plus faible dosage.
En cas d’hémorragies légères ou de tendance aux hémorragies
La quantité, la fréquence et la durée d’administration sont fixées et adaptées à votre situation personnelle par votre médecin.
Normalement le dosage s’élève à 0,1 à 0,5 ml (1 à 5 mg) de solution injectable et buvable de Konakion MM.
Aux doses faibles, on peut également avoir recours à une ou plusieurs ampoules de Konakion MM paediatric à 2 mg dans 0,2 ml (même solution que Konakion MM à 10 mg dans 1 ml), en utilisant éventuellement la pipette pour l’administration orale jointe à l’emballage de Konakion MM paediatric.
Mode d’emploi pour l’administration orale
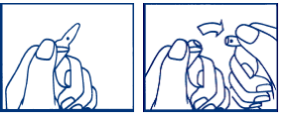
Figure 1 Figure 2
L’administration orale de Konakion MM peut être effectuée à l’aide d’une seringue comme suit:
Ouverture des ampoules:
Fig. 1: Tenez le cylindre en verre de l’ampoule (corps de l’ampoule) entre deux doigts, le point coloré étant dirigé vers le haut et vers vous. Tapotez et secouez la partie supérieure de l’ampoule pour faire descendre la solution s’y trouvant.
Fig. 2: Cassez l’extrémité supérieure de l’ampoule en l’inclinant vers l’arrière. Afin de ne pas vous couper, utilisez p.ex. un tampon pour ouvrir l’ampoule.
Prélevez de l’ampoule le volume requis à l’aide de la seringue munie de son aiguille. Retirez ensuite l’aiguille de la seringue et appliquez le contenu de la seringue directement dans la bouche; rincez-vous avec du liquide et avalez.
Remarque pour l’administration parentérale
Tout éventuelle administration intraveineuse doit être réalisée par votre médecin ou une personne qualifiée.
Remarques générales
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Konakion MM peut-il provoquer ?
La prise ou l’utilisation de Konakion MM peut provoquer les effets secondaires suivants :
Dans de rares cas, des réactions éventuellement de forte intensité, telles qu’inflammation, atrophie tissulaire ou mort de cellules tissulaires, peuvent survenir au niveau du site d’injection. Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
A quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention
«EXP» sur le récipient. Ne pas conserver au-dessus de 25 °C. Conserver les ampoules dans l’emballage d’origine pour les protéger de la lumière. Conserver hors de la portée des enfants.
Pour des raisons de stabilité, les quantités restantes dans les ampoules ouvertes ne peuvent être conservées et doivent être jetées.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient Konakion MM ?
1 ml de solution injectable et buvable de Konakion MM contient :
Principe actif
10 mg de phytomenadionum (vitamine K1)
Excipients
Acidum glycocholicum, natrii hydroxidum, lecithinum (produit à partir d’huile de soja génétiquement modifié), acidum hydrochloricum, aqua ad iniectabile
Numéro d’autorisation
48112 (Swissmedic)
Où obtenez-vous Konakion MM ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Konakion MM, solution injectable et buvable: emballage de 5 ampoules à 10 mg/1 ml.
Titulaire de l’autorisation
CPS Cito Pharma Services GmbH, 8610 Uster
Cette notice d’emballage a été vérifiée pour la dernière fois en janvier 2022 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 04.05.2023, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère mise à jour de cette page depuis le lancement début 2021 de cette rubrique. MAJ 1 (04.05.2023)
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


