AMGEVITA 40 mg solution injectable en stylo prérempli
Information destinée aux patients en Suisse
Qu’est-ce que AMGEVITA et quand doit-il être utilisé ?
AMGEVITA est un médicament qui limite le processus inflammatoire dans le traitement des maladies suivantes: polyarthrite rhumatoïde, arthrite psoriasique, maladie de Bechterew (spondylarthrite ankylosante), maladie de Crohn, colite ulcéreuse, psoriasis, maladie de Verneuil et uvéite non infectieuse chez les adultes ainsi qu’arthrite juvénile idiopathique polyarticulaire chez les enfants et les adolescents de 4 à 17 ans, maladie de Crohn chez les enfants et les adolescents de 6 à 17 ans et psoriasis à partir de l’âge de 6 ans. Le principe actif, l’adalimumab, est un anticorps monoclonal humain produit par des méthodes biotechnologiques (technologie de l’ADN recombinant). Les anticorps monoclonaux sont des protéines qui reconnaissent d’autres protéines spécifiques et s’y lient. L’adalimumab agit en se liant à une protéine spécifique (le facteur de nécrose tumorale ou TNFα) qui est présente en hautes concentrations lors de maladies inflammatoires telles que la polyarthrite rhumatoïde, l’arthrite juvénile idiopathique polyarticulaire, l’arthrite psoriasique, la maladie de Bechterew (spondylarthrite ankylosante), la maladie de Crohn, la colite ulcéreuse, le psoriasis, la maladie de Verneuil et l’uvéite non infectieuse.
Polyarthrite rhumatoïde
La polyarthrite rhumatoïde est une maladie inflammatoire des articulations. AMGEVITA est un médicament destiné au traitement de la polyarthrite rhumatoïde active modérée à sévère et indiqué lorsque la réponse aux autres agents antirhumatismaux modificateurs de la maladie (p.ex. le méthotrexate, la sulfasalazine ou l’hydroxychloroquinine) n’est pas suffisante pour limiter les douleurs et les œdèmes des articulations, protéger ces dernières contre (ou ralentir) l’effet néfaste de la polyarthrite rhumatoïde sur les cartilages et les os des articulations et améliorer la fonction physique corporelle.
AMGEVITA peut aussi être utilisé lorsque la polyarthrite rhumatoïde vient d’être diagnostiquée et n’a pas été auparavant traitée par le méthotrexate.
Arthrite psoriasique
L’arthrite psoriasique est une maladie inflammatoire des articulations qui peut survenir en liaison avec le psoriasis. Si vous souffrez d’arthrite psoriasique, votre médecin vous a déjà prescrit d’autres médicaments modifiant l’évolution de la maladie, comme par exemple, le méthotrexate, auquel votre réponse n’était pas suffisante. AMGEVITA ralentit l’effet délétère de l’arthrite psoriasique sur le cartilage et les os des articulations et améliore les capacités fonctionnelles physiques.
Maladie de Bechterew (spondylarthrite ankylosante)
La maladie de Bechterew (spondylarthrite ankylosante) est une maladie inflammatoire de la colonne vertébrale. Si vous souffrez de la maladie de Bechterew (spondylarthrite ankylosante), votre médecin vous a déjà prescrit d’autres médicaments. Si vous n’avez pas répondu suffisamment à ces médicaments, AMGEVITA vous a été prescrit pour réduire les signes et symptômes de votre maladie.
Maladie de Crohn chez l’adulte, l’enfant et l’adolescent
La maladie de Crohn est une maladie inflammatoire des voies digestives. Si vous ou votre enfant souffrez de la maladie de Crohn, le médecin a déjà prescrit d’autres médicaments modifiant son évolution, auxquels vous ou votre enfant n’avez pas répondu de façon satisfaisante.
L’adalimumab n’a pas été examiné chez l’enfant de moins de 6 ans atteint de la maladie de Crohn.
Colite ulcéreuse
La colite ulcéreuse est une maladie inflammatoire de l’intestin. Si vous souffrez de colite ulcéreuse, d’autres médicaments vous ont déjà été prescrits. Si vous n’avez pas atteint une réponse suffisante à ces médicaments, AMGEVITA vous a été prescrit pour réduire les signes et symptômes de votre maladie.
Psoriasis chez l’adulte, l’enfant et l’adolescent
Le psoriasis est une maladie inflammatoire de la peau. Si vous êtes adulte et souffrez de psoriasis en plaques chronique modéré à sévère, AMGEVITA vous a été prescrit pour réduire les signes et symptômes de votre maladie.
Un traitement par AMGEVITA est prescrit à votre enfant si celui-ci souffre d’une forme sévère de psoriasis en plaques chronique et que les autres traitements ne sont pas efficaces ou ne sont pas appropriés dans son cas.
L’adalimumab n’a pas été étudié chez les enfants de moins de 6 ans atteints de psoriasis en plaques.
Maladie de Verneuil
La maladie de Verneuil (également appelée hidradénite suppurée) est une maladie inflammatoire chronique et souvent douloureuse de la peau. Ses symptômes englobent des nodules et furoncles (abcès) sensibles qui peuvent être purulents.
AMGEVITA est utilisé chez l’adulte pour traiter la maladie de Verneuil en cas de réponse insatisfaisante de cette maladie à un traitement antibiotique.
Uvéite non infectieuse
L’uvéite non infectieuse est une maladie inflammatoire de l’œil qui n’est pas due à une infection. Cette inflammation peut détériorer la capacité visuelle et/ou causer l’apparition de corps flottants du vitré («mouches volantes» ou structures filiformes flottantes perçues dans le champ visuel) de l’œil. Des douleurs ou une sensibilité excessive à la lumière peuvent également se manifester. AMGEVITA est utilisé pour traiter l’uvéite non infectieuse affectant les parties moyenne et postérieure de l’œil et la panuvéite.
Arthrite juvénile idiopathique polyarticulaire
L’arthrite juvénile idiopathique polyarticulaire est une maladie inflammatoire affectant une ou plusieurs articulations. Le diagnostic est généralement établi chez des enfants de moins de 16 ans. Il est possible que l’on prescrive d’abord à votre enfant un traitement par d’autres médicaments modificateurs de la maladie tels que le méthotrexate. Si votre enfant ne répond pas suffisamment à ces médicaments, AMGEVITA lui sera administré pour traiter son arthrite juvénile idiopathique polyarticulaire.
L’adalimumab n’a pas été étudié chez les enfants de moins de 4 ans.
Vous-même ou votre enfant ne devez utiliser AMGEVITA que sur prescription du médecin.
Quand AMGEVITA ne doit-il pas être utilisé ?
Vous-même ou votre enfant ne devez pas prendre AMGEVITA si vous présentez une hypersensibilité (allergie) à l’adalimumab ou à un autre composant d’AMGEVITA.
Si vous ou votre enfant souffrez d’une infection grave, y compris d’une tuberculose active (voir «Quelles sont les précautions à observer lors de l’utilisation d’AMGEVITA ?»). Si vous ou votre enfant présentez des symptômes infectieux tels que fièvre, plaies, abattement ou problèmes dentaires, il est important que vous en informiez votre médecin/le médecin de votre enfant.
Si vous souffrez/si votre enfant souffre de sclérose en plaques ou de névrite optique (inflammation du nerf optique) ainsi que de troubles sensoriels, votre médecin/le médecin de votre enfant décidera si vous pouvez/si votre enfant peut utiliser AMGEVITA.
Si vous souffrez/si votre enfant souffre d’insuffisance cardiaque modérée ou grave. Si vous avez eu/si votre enfant a eu par le passé une maladie cardiaque grave ou si vous en souffrez/si votre enfant en souffre encore, il est important que vous en informiez votre médecin/le médecin de votre enfant (voir «Quelles sont les précautions à observer lors de l’utilisation d’AMGEVITA ?»).
Quelles sont les précautions à observer lors de l’utilisation d’AMGEVITA ?
– Au cours d’un traitement par AMGEVITA, il se peut que vous contractiez/que votre enfant contracte des infections plus facilement. Il peut s’agir d’infections graves, y compris la tuberculose, d’infections provoquées par des virus, des champignons ou des bactéries, d’autres infections et d’intoxication sanguine, qui, dans de rares cas, peuvent présenter un risque mortel. Il est très important que vous signaliez à votre médecin/au médecin de votre enfant tout symptôme du type fièvre, plaies, manifestations de fatigue ou problèmes dentaires.
– Si vous souffrez/si votre enfant souffre d’une infection, y compris présente depuis longtemps ou limitée localement (p.ex. ulcère crural), veuillez consulter votre médecin/le médecin de votre enfant avant de commencer le traitement par AMGEVITA. En cas d’incertitude, veuillez consulter votre médecin/le médecin de votre enfant.
– Si vous avez souffert/si votre enfant a souffert par le passé d’infections à répétition ou si vous vous trouvez/si votre enfant se trouve dans une situation augmentant le risque d’infections, veuillez en informer votre médecin/le médecin de votre enfant.
– Informez votre médecin ou le médecin de votre enfant si vous voyagez ou séjournez ou si votre enfant voyage ou séjourne dans des régions touchées par la tuberculose ou des infections provoquées par des champignons, telles que l’histoplasmose, la coccidioïdomycose ou la blastomycose.
– Comme des cas de tuberculose ont été rapportés chez des patients traités par l’adalimumab, le médecin recherchera chez vous/chez votre enfant la présence éventuelle de signes et symptômes d’une tuberculose avant le début du traitement par AMGEVITA. Cet examen inclut l’établissement détaillé des antécédents médicaux, une radiographie du thorax et un test à la tuberculine. Il est extrêmement important que vous précisiez à votre médecin/au médecin de votre enfant si vous avez/si votre enfant a déjà été atteint par la tuberculose ou si vous avez/si votre enfant a été en contact étroit avec une personne ayant la tuberculose. Une tuberculose peut se développer pendant le traitement par AMGEVITA, même si vous avez/si votre enfant a reçu un traitement préventif contre la tuberculose. Il est aussi important que vous informiez votre médecin/le médecin de votre enfant des autres médicaments que vous prenez/que prend votre enfant éventuellement. Si, au cours du traitement, des symptômes d’une tuberculose (toux persistante, perte de poids, manque d’entrain, fièvre) ou d’une autre infection surviennent, veuillez le signaler immédiatement à votre médecin/au médecin de votre enfant.
– Si vous êtes/si votre enfant est porteur du virus de l’hépatite B (VHB), si vous souffrez/si votre enfant souffre d’une infection active par ce virus ou si vous présentez/si votre enfant présente un risque accru d’infection par ce virus, veuillez en informer votre médecin/le médecin de votre enfant. AMGEVITA peut entraîner une réactivation du VHB chez les personnes qui en sont porteuses. Dans quelques cas rares, en particulier lors de l’utilisation concomitante de médicaments qui inhibent le système immunitaire, une réactivation de ce virus peut être potentiellement mortelle.
– Avant toute intervention chirurgicale et avant tout traitement dentaire, vous devez informer le médecin que vous suivez/que votre enfant suit un traitement par AMGEVITA.
– Si vous avez ou développez/si votre enfant a ou développe une maladie neurologique, comme par exemple la sclérose en plaques, votre médecin/le médecin de votre enfant décidera si vous devez/si votre enfant doit recevoir ou continuer à recevoir AMGEVITA. Informez immédiatement votre médecin/le médecin de votre enfant si vous remarquez des symptômes tels qu’altération de la vision, faiblesse dans les bras ou les jambes ou sensation d’engourdissement ou de fourmillement dans le corps.
– Si vous avez/si votre enfant a des réactions allergiques (p.ex. sensation d’oppression dans la poitrine, respiration sifflante, vertiges, œdèmes ou éruptions cutanées), vous devez interrompre l’injection d’AMGEVITA et contacter immédiatement votre médecin/le médecin de votre enfant.
– Pendant un traitement par AMGEVITA, certains vaccins (p.ex. vaccin antipolio oral) ne doivent pas être administrés. Veuillez consulter votre médecin/le médecin de votre enfant avant de vous faire vacciner/de faire vacciner votre enfant. Une mise à jour de toutes les vaccinations conformément aux directives applicables est recommandée si possible avant de commencer le traitement par AMGEVITA chez les enfants et adolescents.
– Si vous avez reçu AMGEVITA pendant la grossesse, votre nourrisson présente éventuellement un risque accru d’avoir une infection pendant les 5 mois qui suivent la dernière dose administrée pendant la grossesse. Il est important d’informer le pédiatre et les autres membres du corps médical qu’AMGEVITA a été utilisé pendant la grossesse afin que ceux-ci puissent décider si le nourrisson peut être vacciné (p.ex. vaccin BCG).
– Si vous souffrez/si votre enfant souffre d’insuffisance cardiaque légère et si vous êtes traité(e)/si votre enfant est traité par AMGEVITA, votre médecin/le médecin de votre enfant doit surveiller régulièrement votre état cardiaque/l’état cardiaque de votre enfant. Si vous avez eu/si votre enfant a eu par le passé une maladie cardiaque grave ou si vous en souffrez/si votre enfant en souffre encore, il est important que vous en informiez votre médecin/le médecin de votre enfant. Contactez immédiatement votre médecin/le médecin de votre enfant si vous ou votre enfant présentez de nouveaux signes d’insuffisance cardiaque ou une aggravation des signes (p.ex. essoufflement ou œdème des pieds). Le médecin décidera si vous pouvez/si votre enfant peut continuer le traitement par AMGEVITA.
– Informez votre médecin/le médecin de votre enfant si des symptômes comme par exemple une fièvre persistante, des hématomes, des saignements et des pâleurs apparaissent. Ceci est le signe d’un trouble sanguin.
– Parmi les patients utilisant de l’adalimumab ou d’autres inhibiteurs du TNF, des cas rares de certains types de cancer ont été rapportés. Les patients présentant une forme évolutive grave de polyarthrite rhumatoïde et chez lesquels cette maladie est présente depuis longtemps peuvent présenter un risque supérieur à la moyenne de développement d’un lymphome (une forme de cancer touchant le système lymphatique) et d’une leucémie (une forme de cancer touchant le sang et la moelle osseuse). Si vous ou votre enfant utilisez AMGEVITA, votre risque/son risque peut éventuellement être accru. Dans de rares cas, une forme particulière et sévère de lymphome a été observée chez des patients traités par l’adalimumab. Certains de ces patients ont été traités simultanément par l’azathioprine ou la 6-mercaptopurine (médicament pour le traitement d’affections intestinales inflammatoires). Informez votre médecin/le médecin de votre enfant si vous prenez/si votre enfant prend de l’azathioprine ou de la 6-mercaptopurine. De plus, on a observé dans de rares cas, chez des patients suivant un traitement par l’adalimumab, des tumeurs cutanées qui n’étaient pas des mélanomes.
– Sodium: ce médicament contient moins de 1 mmol de sodium (23 mg) par dose de 0,8 ml, c’est-à-dire qu’il est quasiment «sans sodium».
Utilisation d’autres médicaments:
AMGEVITA peut être utilisé avec le méthotrexate ou d’autres agents antirhumatismaux modificateurs de la maladie (sulfasalazine, hydroxychloroquinine, léflunomide et préparations injectables à base de sels d’or), avec des corticoïdes ou des antalgiques (anti-inflammatoires non stéroïdiens inclus).
Vous ne devez pas/votre enfant ne doit pas utiliser AMGEVITA concomitamment avec des médicaments contenant de l’anakinra ou de l’abatacept comme principes actifs.
Ce médicament peut affecter les réactions, l’aptitude à conduire et la capacité à utiliser des outils ou des machines.
Veuillez informer le médecin ou le pharmacien si vous souffrez/si votre enfant souffre d’une autre maladie, si vous êtes/si votre enfant est allergique ou si vous prenez ou utilisez déjà/si votre enfant prend ou utilise déjà d’autres médicaments en usage interne ou externe (même en automédication!).
AMGEVITA peut-il être utilisé pendant la grossesse ou l’allaitement ?
– Parlez-en à votre médecin si vous êtes enceinte ou envisagez une grossesse, étant donné qu’AMGEVITA ne doit être utilisé pendant la grossesse qu’en cas de nécessité absolue.
– Pour éviter une grossesse, vous devez prévoir l’utilisation d’une méthode de contraception appropriée et l’appliquer pendant le traitement et jusqu’au moins cinq mois après la dernière dose d’AMGEVITA.
– Si AMGEVITA a été utilisé pendant la grossesse, le nourrisson présente éventuellement un risque accru d’avoir une infection pendant les 5 premiers mois qui suivent la dernière dose administrée pendant la grossesse.
– Il est important d’informer le pédiatre et les autres membres du corps médical qu’AMGEVITA a été utilisé pendant la grossesse afin que ceux-ci puissent décider si le nourrisson peut être vacciné (p.ex. vaccin BCG).
– Il a été rapporté que de très faibles quantités d’adalimumab passent dans le lait maternel. Parlez-en à votre médecin si vous allaitez ou envisagez d’allaiter.
Comment utiliser AMGEVITA ?
AMGEVITA doit être utilisé en respectant très exactement la prescription du médecin. Si vous avez des doutes, consultez le médecin ou le pharmacien.
Adultes
La dose habituelle d’adalimumab pour les patients adultes souffrant de polyarthrite rhumatoïde, d’arthrite psoriasique et de maladie de Bechterew (spondylarthrite ankylosante) est de 40 mg (une injection de 40 mg) toutes les deux semaines, en injection sous-cutanée, sous la peau. Votre médecin peut aussi vous prescrire d’autres agents antirhumatismaux modificateurs de la maladie à utiliser avec AMGEVITA.
Si vous suivez un traitement par AMGEVITA contre la polyarthrite rhumatoïde sans méthotrexate, votre médecin peut décider de vous prescrire 40 mg d’adalimumab (une injection de 40 mg) une fois par semaine ou 80 mg (deux injections de 40 mg) toutes les deux semaines.
Le schéma posologique usuel pour le traitement de la maladie de Crohn commence la semaine 0 par une dose de 160 mg (soit quatre injections de 40 mg administrées le même jour, soit deux injections de 40 mg par jour pendant deux jours consécutifs). La deuxième dose, administrée la semaine 2, est de 80 mg (deux injections de 40 mg). Par la suite, le médicament est administré à la dose de 40 mg (une injection de 40 mg) une semaine sur deux.
La posologie recommandée pour le traitement de la colite ulcéreuse est de 160 mg la semaine 0 (sous forme de quatre injections de 40 mg le même jour ou de deux injections de 40 mg par jour deux jours de suite), de 80 mg (deux injections de 40 mg) la semaine 2, puis de 40 mg (une injection de 40 mg) une semaine sur deux par la suite. Selon votre réponse au traitement, votre médecin pourra si nécessaire augmenter votre dose à 40 mg (une injection de 40 mg) par semaine ou 80 mg (deux injections de 40 mg) toutes les deux semaines.
Le schéma posologique usuel pour les patients adultes souffrant de psoriasis est une dose initiale de 80 mg (deux injections de 40 mg), suivie d’une dose de 40 mg (une injection de 40 mg) toutes les deux semaines, en commençant une semaine après l’administration de la dose initiale. Selon la façon dont vous répondez au traitement, votre médecin peut éventuellement augmenter votre dose à 40 mg (une injection de 40 mg) par semaine ou 80 mg (deux injections de 40 mg) toutes les deux semaines.
Schéma posologique usuel chez les patients adultes atteints de la maladie de Verneuil: dose initiale de 160 mg (quatre injections de 40 mg le même jour ou deux injections de 40 mg par jour pendant 2 jours consécutifs) la semaine 0, de 80 mg (deux injections de 40 mg) la semaine 2. À partir de la semaine 4, la dose sera de 40 mg (une injection de 40 mg) une fois par semaine ou de 80 mg (deux injections de 40 mg) toutes les deux semaines.
Le schéma posologique usuel chez les patients adultes atteints d’uvéite non infectieuse comprend une dose initiale de 80 mg (deux injections de 40 mg), suivie d’une dose de 40 mg (une injection de 40 mg) toutes les deux semaines, en commençant une semaine après l’administration de la dose initiale.
Enfants et adolescents
Arthrite juvénile idiopathique polyarticulaire (4 à 17 ans)
La dose recommandée d’AMGEVITA pour les patients atteints d’arthrite juvénile idiopathique polyarticulaire dépend du poids corporel de l’enfant.
– Enfants et adolescents pesant entre 10 kg et moins de 30 kg:
La dose d’AMGEVITA recommandée est de 20 mg* une semaine sur deux.
– Enfants et adolescents pesant 30 kg et plus:
La dose d’AMGEVITA recommandée est de 40 mg (une injection de 40 mg) une semaine sur deux.
Enfants ou adolescents atteints de la maladie de Crohn (6 à 17 ans)
La dose recommandée d’AMGEVITA pour les patients atteints de la maladie de Crohn dépend du poids de l’enfant et de la sévérité de sa maladie.
– Enfants et adolescents pesant moins de 40 kg:
La dose initiale est de 80 mg (deux injections de 40 mg), suivie d’une dose de 40 mg (une injection de 40 mg) deux semaines plus tard. Ensuite, la dose est de 20 mg* une semaine sur deux. Selon la réponse de votre enfant au traitement, le médecin pourra si nécessaire augmenter la dose à 20 mg* par semaine.
La dose prescrite par le médecin peut différer du schéma posologique décrit ci-dessus.
– Enfants et adolescents pesant 40 kg et plus:
La dose initiale est de 160 mg (quatre injections de 40 mg le même jour ou deux injections de 40 mg par jour pendant 2 jours consécutifs), suivie d’une dose de 80 mg (deux injections de 40 mg) deux semaines plus tard. Ensuite, la dose est de 20 mg* ou 40 mg (une injection de 40 mg) une semaine sur deux. Selon la réponse de votre enfant au traitement, le médecin pourra si nécessaire augmenter la dose à 20 mg* ou 40 mg (une injection de 40 mg) par semaine. Pour les enfants dont la dose est augmentée à 40 mg (une injection de 40 mg) chaque semaine, une alternative consiste à administrer 80 mg (deux injections de 40 mg) une semaine sur deux.
Enfants et adolescents atteints de psoriasis (à partir de 6 ans)
La dose recommandée d’AMGEVITA chez les patients atteints de psoriasis dépend du poids de l’enfant.
– Enfants et adolescents pesant entre 15 kg et moins de 30 kg:
La dose initiale recommandée d’AMGEVITA est de 20 mg*, suivie de 20 mg* une semaine plus tard. Par la suite, la posologie est de 20 mg* une semaine sur deux.
– Enfants et adolescents pesant 30 kg et plus:
La dose initiale recommandée d’AMGEVITA est de 40 mg (une injection de 40 mg), suivie de 40 mg (une injection de 40 mg) une semaine plus tard. Par la suite, la posologie est de 40 mg (une injection de 40 mg) une semaine sur deux.
*Utilisation d’une dose inférieure à 40 mg d’AMGEVITA par administration
Pour l’utilisation d’une dose inférieure à 40 mg d’AMGEVITA par administration, la seringue préremplie de 20 mg (pour l’utilisation chez les enfants et les adolescents) doit être utilisée.
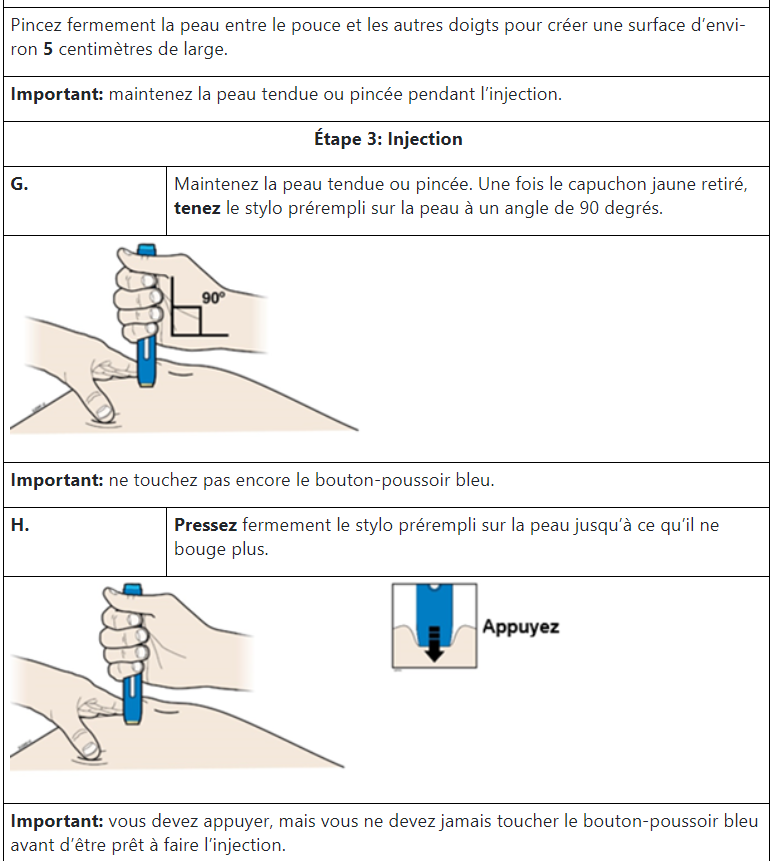
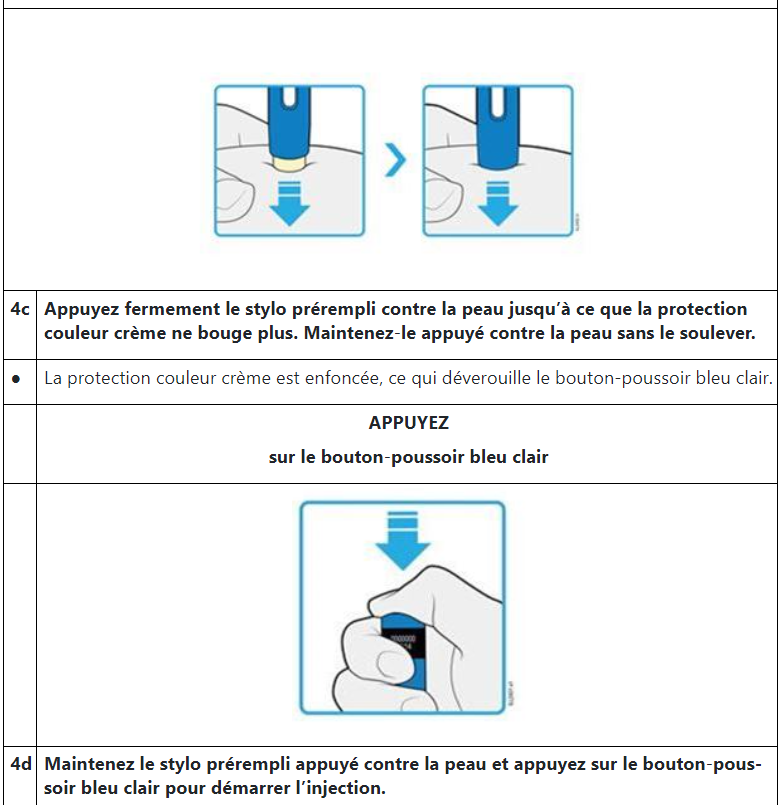
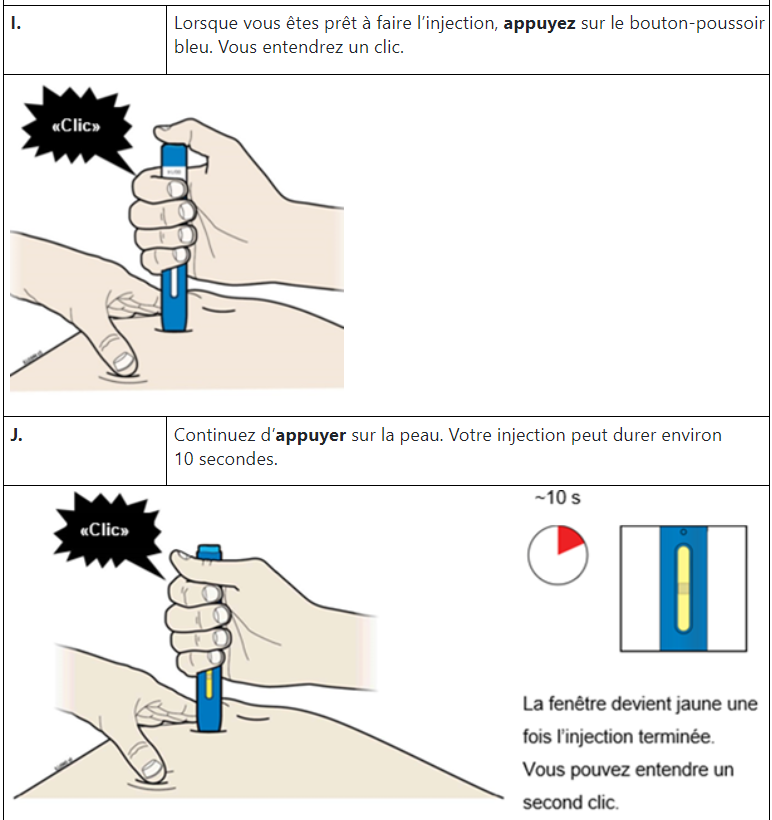
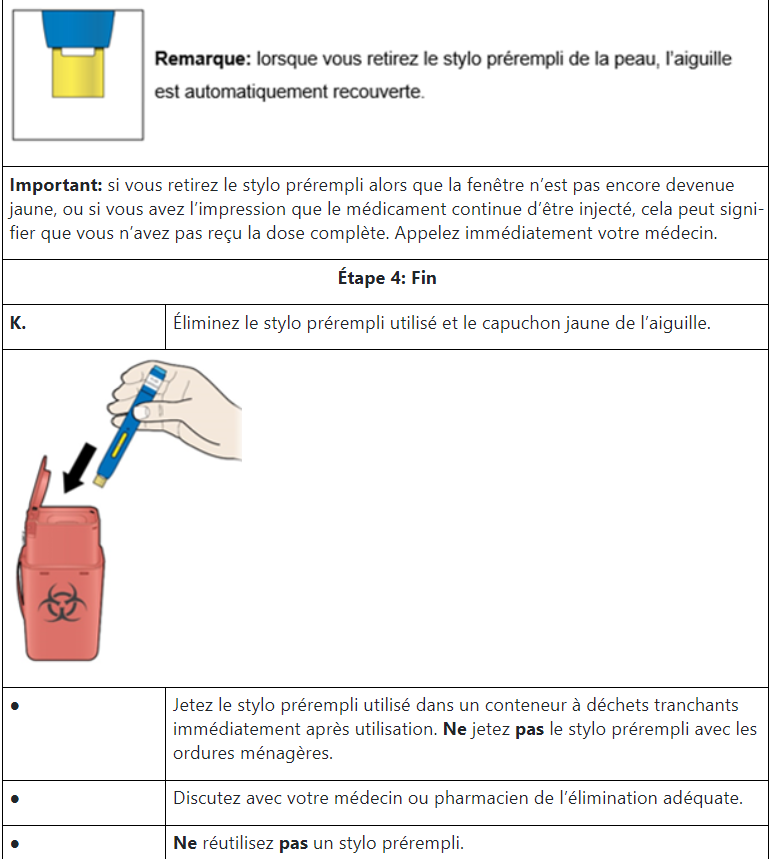
Auto-injection
Après une formation sur l’auto-injection, vous pourrez pratiquer vous-même l’injection ou une autre personne formée pourra la pratiquer pour vous (p.ex. un membre de votre famille ou un ami); votre médecin ou son assistant peut aussi faire l’injection. Vous trouverez à la fin de la présente notice des instructions détaillées pour l’auto-injection. Vous devez vous injecter AMGEVITA/injecter AMGEVITA à votre enfant aussi longtemps que votre médecin/le médecin de votre enfant l’a prescrit.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous au médecin ou au pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Si vous avez utilisé plus d’AMGEVITA que vous ne le deviez:
Si, par erreur, vous vous êtes injecté AMGEVITA/vous avez injecté AMGEVITA à votre enfant plus souvent que prescrit par le médecin, consultez votre médecin/le médecin de votre enfant. Prenez toujours avec vous l’emballage d’origine et le stylo prérempli, même s’il est vide.
Si vous avez oublié l’injection d’AMGEVITA:
Si vous oubliez une injection, vous devez injecter la dose suivante d’AMGEVITA dès que vous y pensez. Injectez ensuite la dose suivante, comme d’habitude, le jour où elle était prévue à l’origine, comme si vous n’aviez pas oublié la dose précédente.
Quels effets secondaires AMGEVITA peut-il provoquer ?
L’utilisation d’AMGEVITA peut provoquer les effets secondaires suivants:
Si vous remarquez/si votre enfant remarque l’un des signes suivants, veuillez en informer immédiatement le médecin ou le pharmacien:
– Éruption cutanée sévère, urticaire ou autres signes d’une réaction allergique
– Gonflement du visage, des mains ou des pieds
– Difficultés à respirer ou à avaler
– Essoufflement à l’effort ou au repos
– Signes et symptômes pouvant signaler une maladie hématopoïétique: fièvre durable, épanchements sanguins, pâleur
– Signes de problèmes au foie, comme p.ex. coloration jaune des yeux ou de la peau, urines brun foncé, démangeaisons, perte d’appétit ou nausées.
Si vous remarquez/si votre enfant remarque l’un des signes suivants, veuillez en informer le plus rapidement possible le médecin ou le pharmacien:
– Signes d’une infection comme p.ex. fièvre, malaises, plaies, problèmes dentaires, brûlure à la miction
– Sensation de faiblesse ou de fatigue
– Toux
– Démangeaisons
– Engourdissement
– Vision double
– Faiblesse des bras ou des jambes
– Une bosse ou des plaies ouvertes qui ne guérissent pas.
Les symptômes décrits ci-dessus peuvent être des signes des effets secondaires présentés ci-dessous et qui ont été observés avec l’adalimumab (le principe actif d’AMGEVITA): très fréquents (≥1 patient/10), fréquents (≥1 patient/100 et <1 patient/10), occasionnels (≥1 patient/1000 et <1 patient/100), rares (<1 patient/1000), cas isolés (la fréquence ne peut être déterminée à partir des données disponibles).
Très fréquents
Réactions au site d’injection (y compris douleurs, gonflement, rougeur ou démangeaisons).
Chez l’enfant: infections.
Fréquents
Infections des voies respiratoires (telles que refroidissement, rhume accompagné de rhinorrhée, infection des sinus, infection de la gorge, infection pulmonaire), infections de la bouche (y compris herpès), infections de la peau (y compris inflammation du lit de l’ongle et zona), infections des voies urinaires (p.ex. sensation de brûlure lors de la miction, miction impérieuse accrue), infections sévères (y compris septicémie et infections fongiques), une diminution du nombre des globules blancs (p.ex. sensibilité accrue aux infections), maux de tête, troubles de la sensibilité (comme picotements, fourmillements ou sensation d’insensibilité), obnubilation, toux, diarrhée, douleurs abdominales, nausées, maux de gorge, éruption et inflammation cutanée, arthrite, douleurs musculaires et osseuses, fatigue.
Chez l’enfant: hypersensibilité.
Occasionnels
Infections des oreilles, infections intestinales (y compris inflammation du foie), infections articulaires, infections des organes reproducteurs, mycoses, infections bactériennes, abcès, néoformations bénignes, anémie (p.ex. symptômes de fatigue, pâleur des lèvres et des gencives), hypersensibilité, réactions allergiques sévères (y compris angiœdème, un gonflement de la peau et/ou de la muqueuse), manque d’appétit, troubles de l’appétit, sautes d’humeur (y compris dépression), sensation d’angoisse, troubles du sommeil, tremblement, troubles de la conscience, événements cérébrovasculaires, inflammation des yeux, glaucome, gonflement des yeux, troubles des oreilles, vertiges, acouphènes, palpitations, hypertension, infarctus du myocarde, rougissement, asthme, essoufflement, trouble de la voix, écoulement nasal, râles, saignements de nez, saignements gastro-intestinaux, troubles digestifs (y compris indigestion, aigreurs d’estomac), ulcères de la bouche, maladies inflammatoires intestinales, affections hépatiques, perte de cheveux, acné, psoriasis (y compris sur la paume des mains et/ou la plante des pieds et/ou sous forme de vésicules), eczéma, hématomes, transpiration accrue, cicatrices, démangeaisons, crampes musculaires, troubles de la vessie et de l’urètre, troubles vulvo-vaginaux, troubles menstruels, douleurs thoraciques, fièvre, rétention d’eau dans les tissus (œdèmes), symptômes pseudo-grippaux, frissons, augmentation de poids, guérison des plaies retardée.
Rares
Infections localisées dans le bas-ventre (y compris inflammations du côlon), infections oculaires (y compris infection herpétique), infections survenant chez des personnes dont le système immunitaire est affaibli (p.ex. tuberculose), méningite causée par un virus, infection parasitaire sévère, cancer (y compris cancer de la peau et cancer des ganglions lymphatiques), leucémie, troubles immunitaires pouvant concerner le poumon, la peau et les ganglions lymphatiques (se manifestant le plus souvent sous forme de sarcoïdose), réactions allergiques, insuffisance de la fonction thyroïdienne (p.ex. apathie, grande fatigabilité, sensation fréquente d’avoir trop froid, prise de poids), goitre, troubles du système nerveux (tels que syndrome de Guillain-Barré [pouvant causer une faiblesse musculaire, des anomalies sensorielles et des fourmillements dans les bras et le torse], névrite optique [inflammation des nerfs oculaires], sclérose en plaques), anomalies des réflexes, pertes de conscience, troubles de l’équilibre, troubles de l’attention, paralysie du visage, affections nerveuses (p.ex. sclérose en plaques), inflammation de la paupière, inflammation du nerf optique, vue double, inflammation de l’iris de l’œil, perte de l’ouïe, problèmes cardiaques, arrêt cardiaque, faiblesse cardiaque non contrôlable, obstruction des vaisseaux coronaires, renfoncement dans la paroi d’une artère principale, sténose de vaisseaux sanguins, inflammation de vaisseaux sanguins de grand ou de petit calibre (vascularite), hématomes, inflammation et caillot sanguin dans une veine, gonflements dans la région de la gorge, maladies pulmonaires, irritations de la gorge, formation de caillots sanguins dans les vaisseaux sanguins du poumon, constipation, pancréatite, problèmes de déglutition, problèmes dentaires, saignements des gencives, inflammations des lèvres, gonflement du visage, perforation de l’intestin, calculs biliaires, inflammation du foie, réactivation d’une hépatite virale, insuffisance aiguë du foie, anomalies des cheveux et des ongles, irritations de la peau, inflammation de vaisseaux sanguins de la peau (vascularite cutanée), lupus érythémateux disséminé et syndrome de type lupus (p.ex. perte de poids, fatigue, fièvre, éruptions cutanées et troubles articulaires), atrophie musculaire anormale, inflammations des tendons et des muscles squelettiques, sensation de lourdeur, douleurs rénales, insuffisance rénale, maladies de la poitrine, impuissance sexuelle, troubles utérins, inflammations, énergie accrue, sensation anormale, inflammation des muqueuses, sensation de chaleur, éruption cutanée rouge et violette prurigineuse.
Cas isolés
Carcinome à cellules de Merkel (une forme de cancer de la peau), lymphome hépatosplénique à lymphocytes T (un type de leucémie surtout chez les jeunes adultes), aggravation des symptômes de la dermatomyosite (une maladie du système immunitaire avec des symptômes tels que des douleurs liées aux mouvements, des rougeurs, une accumulation de liquide sous la peau), éruption cutanée pouvant entraîner une formation sévère de vésicules et une desquamation.
Si vous remarquez des effets secondaires qui ne sont pas mentionnés dans cette notice, veuillez en informer votre médecin/le médecin de votre enfant ou votre pharmacien.
À quoi faut-il encore faire attention ?
Conserver les médicaments hors de la portée des enfants.
Conserver au réfrigérateur (2°C à 8°C). Ne pas congeler. Conserver le stylo prérempli dans son emballage d’origine pour protéger son contenu de la lumière.
AMGEVITA est une solution limpide, incolore à légèrement jaune.
Conditions exceptionnelles de stockage
Si cela est nécessaire (par exemple, lorsque vous voyagez), il est possible de conserver un unique stylo prérempli d’AMGEVITA pendant une durée allant jusqu’à 14 jours à température ambiante (à 25°C maximum) et à l’abri de la lumière, à savoir dans son emballage d’origine. Une fois que le stylo prérempli a été sorti du réfrigérateur et a été conservé à température ambiante, il doit être utilisé dans les 14 jours ou être éliminé, et ce même s’il a été remis au réfrigérateur entre-temps.
Il est donc important de noter la date du premier retrait du réfrigérateur et la date d’élimination.
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Pour de plus amples renseignements, consultez le médecin ou le pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient AMGEVITA ?
Principes actifs
Adalimumab.
Chaque stylo prérempli contient 40 mg d’adalimumab dans 0,8 ml de solution.
Excipients
Acide acétique glacial, saccharose, polysorbate 80 (produit à partir de maïs génétiquement modifié), hydroxyde de sodium et eau pour préparations injectables.
Numéro d’autorisation
67204 (Swissmedic)
Où obtenez-vous AMGEVITA ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Chaque emballage contient un, deux ou six stylo(s) prérempli(s) à usage unique.
Toutes les présentations peuvent ne pas être disponibles sur le marché.
La solution injectable d’AMGEVITA est également disponible en seringue préremplie.
Titulaire de l’autorisation
Amgen Switzerland AG, Risch
Domicile: 6343 Rotkreuz
Cette notice d’emballage a été vérifiée pour la dernière fois en décembre 2023 par l’autorité de contrôle des médicaments (Swissmedic).
Mode d’emploi
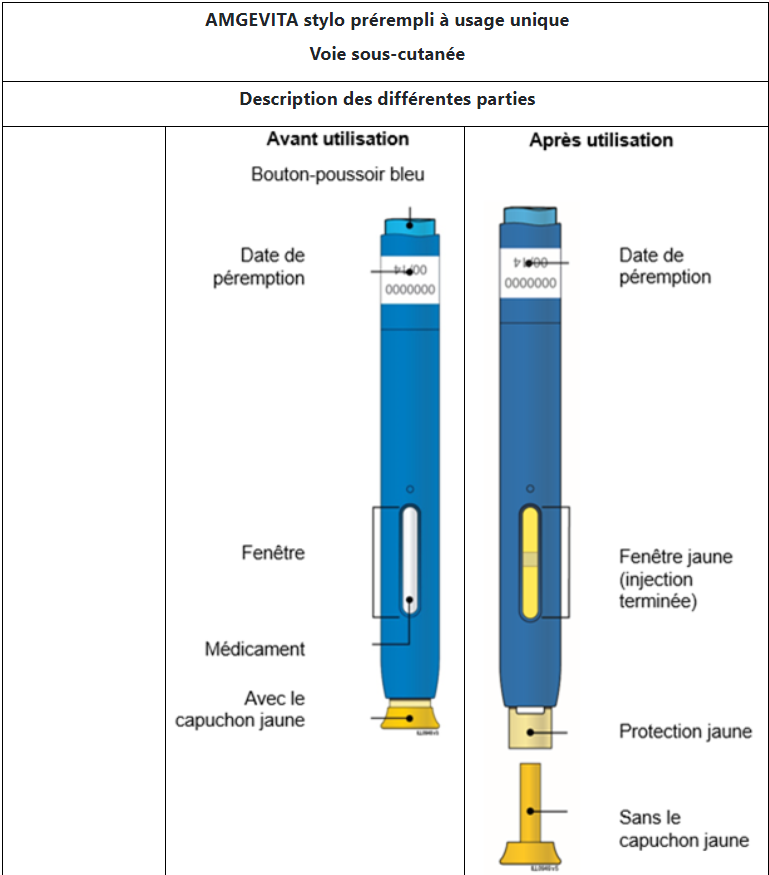


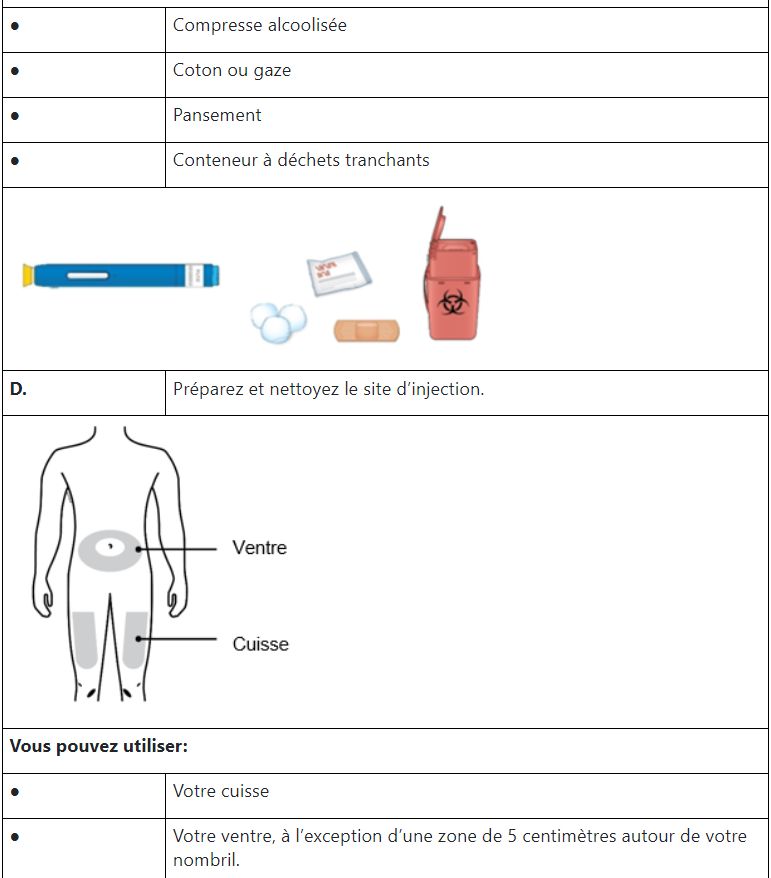
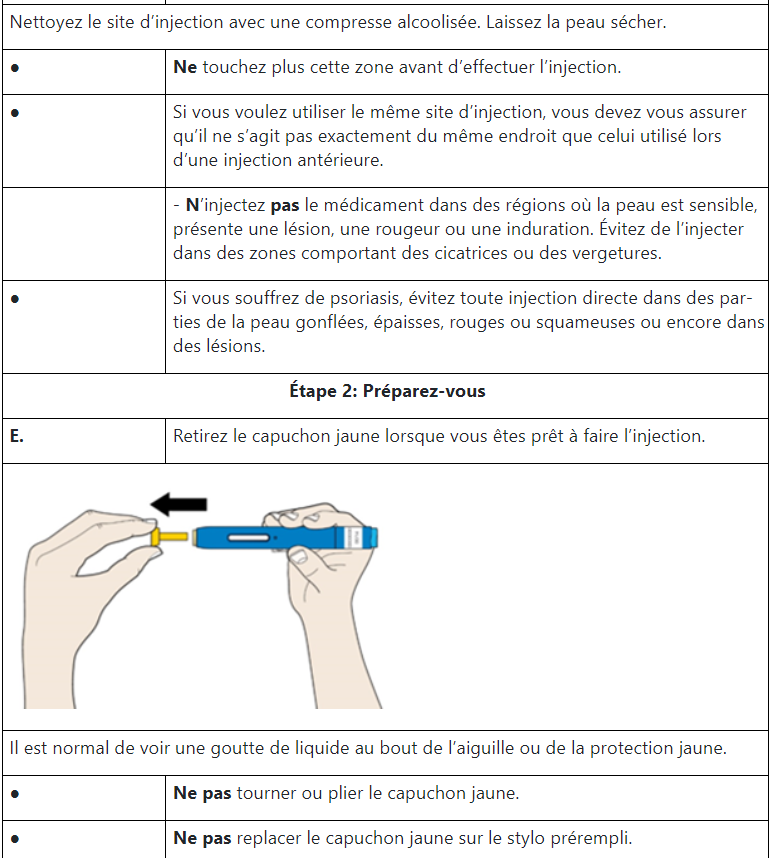
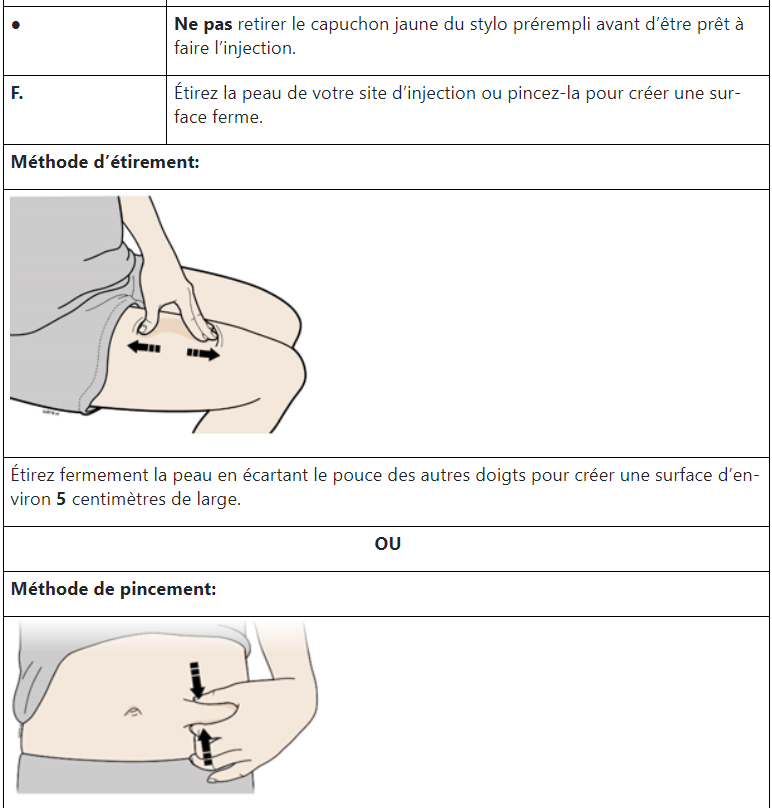

Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 03.05.2024, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans un paragraphe en gras ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 4ème mise à jour de cette page depuis le lancement début 2021 de cette rubrique. Mise à jour 1 (juillet 2021). Mise à jour 2 (décembre 2021). Mise à jour 3 (août 2022).
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


